病例陈述
Scott B. Silverman医师:一名68岁男性因意识错乱恶化入住本院。
患者有高血压和冠心病病史。本次入院前18年曾发生心肌梗死;当时,患者还被诊断患有心房颤动。他曾经服用华法林多年,但在这次入院前10年就停药了。
在本次入院前7周半,患者因失语到另一家医院就诊。他的美国国立卫生研究院卒中量表(NIHSS)评分为3分,该量表评分范围为0~42分,评分较高表示较严重。评分为3分是因为右视野部分丧失、轻度至中度失语、构音障碍。
未静脉输注造影剂的情况下进行的头部计算机断层扫描(CT)未见异常。头颈部CT血管造影显示沿主动脉弓部、左椎动脉起始部、左椎动脉颅内部、颈动脉分叉部、双侧颈内动脉海绵窦部均有钙化性动脉粥样硬化;无显著影响血流动力学的狭窄。患者开始服用阿司匹林和氯吡格雷。患者入院,住院第二日,失语消失。
未静脉给予造影剂的情况下进行的头部磁共振成像(MRI)显示了少许急性梗死小病灶,累及额叶、右内囊后肢和右小脑中脚。在左顶叶皮层下白质也可见一个小的陈旧点状出血灶。
虽然连续远程监测未发现心房颤动证据,但医生认为患者的卒中是由心房颤动引起的心源性栓塞。患者继续服用阿司匹林治疗,停用氯吡格雷,开始用阿哌沙班;之前处方的氨氯地平和赖诺普利抗高血压治疗恢复。住院第二日,患者出院回家。
出院后4天,本次入院前7周,患者因一过性轻度失语转院。头部CT(静脉给予造影剂)和头部MRI(静脉给予和未给予造影剂)的结果与6天前的检查结果相比无变化。患者收缩压<100 mm Hg,其症状被认为是由于灌注不足或之前卒中症状复发所致。停止氨氯地平和赖诺普利治疗,收缩压升高。住院第四日,患者出院回家。
出院后3周,本次入院前3.5周,患者女儿注意到患者意识错乱、嗜睡,将其带到另一家医院进行评估。她报告说,患者新发尿失禁,步态不稳,性格变得孤僻。在没有静脉注射造影剂的情况下进行的头部MRI检查发现双侧半卵圆中心和辐射冠新发急性梗死灶。
Javier M. Romero医师:胸部CT(图1A)显示弥漫性肺气肿改变,左肺下叶可见一带毛刺的肿块(直径1.7 cm),病灶周围肺纹理增粗。腹部CT(图1B)显示左肾前皮层有一个外生性低密度肿块(直径1.6 cm)。
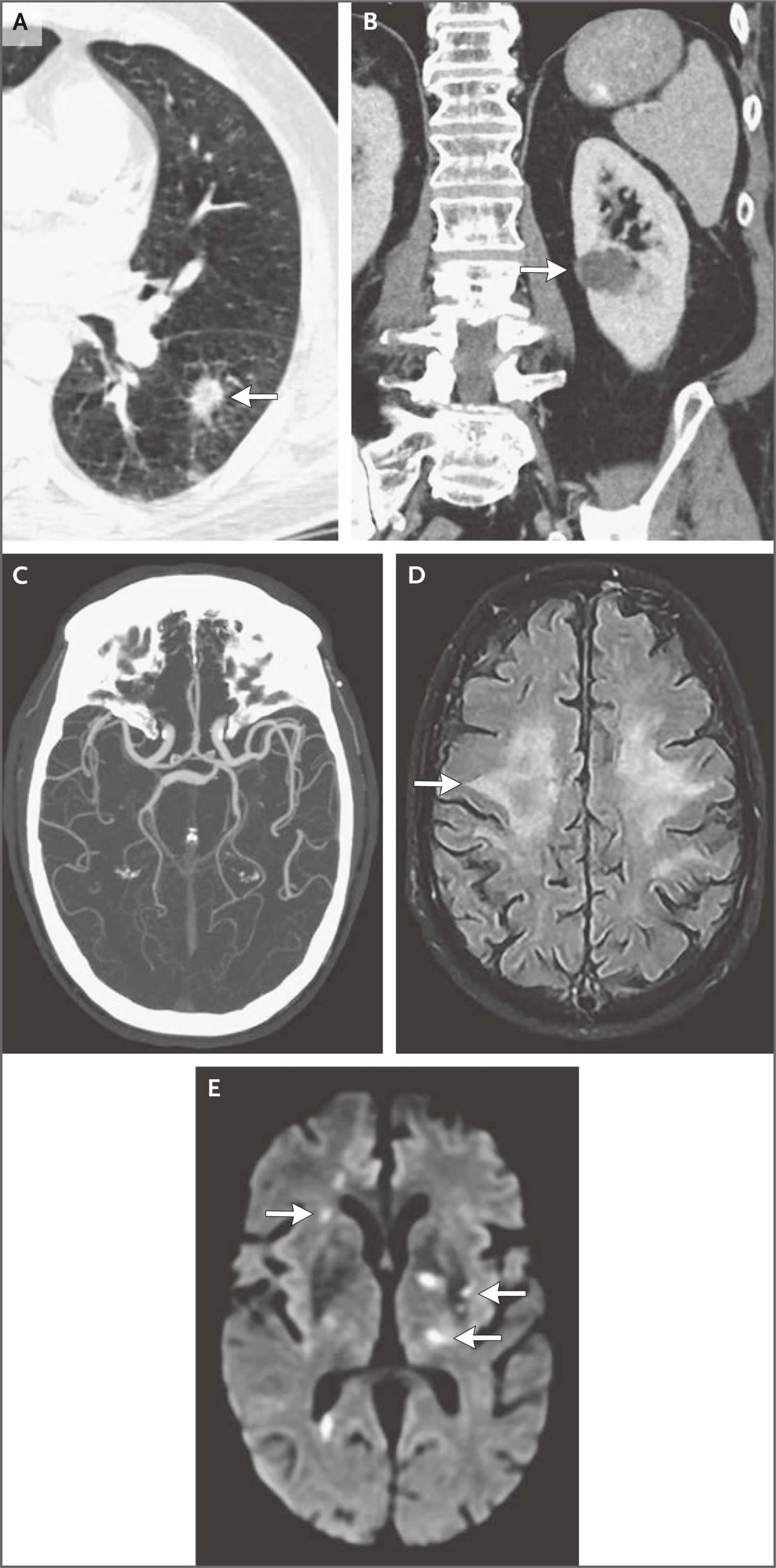
本次入院2周前,在给予造影剂后进行胸部和腹部CT检查。胸部CT轴位图像(图A)显示左肺下叶有一个肿块(直径1.7 cm),病灶周围肺纹理增粗(箭号)。腹部CT冠状位图像(图B)显示左肾前皮层(箭号)有一个外生低密度肿块(直径1.6 cm)。本次入院时进行了头部CT血管造影和MRI检查。CT血管造影最大强度投影图像(图C)显示颈动脉虹吸部钙化,但无影像学上明显的狭窄。MRI轴位液体衰减反转恢复图像(图D)显示脑室周围白质和辐射冠的融合低信号(箭号)。MRI轴位弥散加权图像(图E)显示多个新发急性梗死病灶,涉及左侧丘脑、左侧豆状核和右侧额叶白质(箭号)。
Silverman医师:在住院第四日,患者被转到康复机构,并计划在出院后接受肿瘤学评估。在康复中心住10天后,他离开康复中心回家。
从康复中心出院后3天,本次入院前1周,患者右手和前臂出现麻木和刺痛,患者女儿再次将患者送往另一家医院。检查发现,右上肢平伸试验阳性,指鼻测试时有辨距障碍。头部MRI显示新的急性梗死灶,累及左侧丘脑、右侧额叶皮质下白质和左侧脑室周围白质,但未见出血。停止阿哌沙班治疗,改用依诺肝素治疗。住院第三日,患者出院回家。
出院后5天,患者女儿发现患者吞咽药丸出现困难,意识错乱加重,将患者带到该院急诊科进行评估。患者无法提供额外的病史,但他的女儿报告说,在从另一家医院出院后,他的失语和平衡困难恶化。患者的病史包括高血压、高脂血症、糖尿病和肥胖。用药包括依诺肝素、阿司匹林、阿托伐他汀和二甲双胍。患者无已知药物过敏。患者独自住在波士顿郊区,已经退休。患者已吸烟40年,但最近他把吸烟量从每天一包减少至每天三支。他偶而抽大麻,很少饮酒。他的父亲在三十多岁时患冠心病和心肌梗死。
颞温为36.6°C,血压为158/75 mm Hg,脉搏为70次/分,呼吸频率为18次/分,患者呼吸环境空气时,氧饱和度为98%。体质指数(体重[kg]除以身高[m]的平方)为25.1。患者清醒,能够互动。他能够正确地回答定向问题,但反应迟钝。他讲话很流利,没有言语错乱。他在执行简单命令时有些困难,也无法执行复杂命令。右鼻唇褶活动减少,前额皱纹保留。右上肢平伸试验阳性,右侧轻度偏瘫。其余检查正常。
血电解质和类风湿因子水平正常,肝功能和肾功能检查结果也正常。血红蛋白水平为12.7 g/dL(参考范围,13.5~17.5);全血细胞计数和分类计数的其余部分正常。红细胞沉降率为15 mm/hr(参考范围,0~13)。D-二聚体水平为912 ng/mL(参考值,<500)。尿液分析显示>100个白细胞/高倍视野(参考值,<10)。狼疮抗凝物检测呈阴性,心磷脂和β2-糖蛋白1抗体检测也呈阴性。抗核抗体的滴度为1:160,呈斑点状。采集血样进行了培养。进行了影像学检查。
Romero医师:在静脉给予和未给予造影剂的情况下,头部和颈部的CT血管造影(图1C)显示左侧额叶辐射冠和右侧大脑脚内有局灶性脑软化。动脉粥样硬化改变导致颈动脉和颅内动脉多灶性轻度狭窄。在未静脉给予造影剂的情况下,头部MRI(图1D和1E)可见许多新发急性梗死小病灶,涉及双侧半卵圆中心和辐射冠、左侧丘脑、左侧内囊和豆状核、左侧岛下区、右侧中央前回内侧、右侧额叶前部、额上回和右侧颞叶。在液体衰减反转恢复成像和T2加权成像中,脑室周围和皮质下白质也可见数个散在信号强度增加的斑块,提示中度小血管疾病。
Silverman医师:患者被收入院,并接受肝素静脉给药。住院第2日,经胸超声心动图显示射血分数正常,无瓣膜赘生物,无卵圆孔未闭。血培养未见微生物生长。我们做出了诊断和治疗决定。
鉴别诊断
Aneesh B. Singhal医师:这例68岁的男性患者,在7周内出现多处局灶性和非局灶性神经功能缺损,并伴有认知能力下降。影像学检查显示多灶性缺血性小病灶和白质病变累积。此外,该患者还有可疑为癌症的肺部和肾脏肿块。确定该患者卒中的原因对于评估复发风险和启动适当的预防性治疗非常重要。临床和影像学表现之间的相关性以及缺血性病变的分布提供了重要的诊断线索。脑卒中分类模式1,2有助于考虑该患者脑卒中的潜在机制。
卒中机制
小血管疾病
虽然该患者有小梗死灶,但卒中原因可以排除小血管疾病,因为患者没有腔隙性梗死综合征。由小血管疾病引起的卒中患者通常在脑动脉穿通支分布区域有单一梗死灶;在慢性高血压导致脑动脉穿通支的血管壁透明样变并闭塞3。
心源性栓塞
该患者患有长期心房颤动,这是美国卒中最常见的原因。在初次就诊时,即本次入院前7.5周,患者未接受抗凝治疗,抗凝治疗可降低约60%的卒中风险。他有失语和偏盲,这是左大脑中动脉心源性栓塞的典型表现。然而,影像学检查显示脑深部分散的小梗死灶,而不是心房颤动相关卒中的典型楔形大梗死灶。
几天后失语复发,但影像学检查没有发现新的脑部病变。失语归因于卒中后复发,对失语作为既往卒的结局之一,过去十年对此已有定论4。该患者的第三次和第四次入院是由于他的意识错乱以及情绪和步态的变化,这些不符合典型的临床卒中综合征5。相反,他可能患有栓塞性脑病6。
快速进展的临床表现和梗死分布提示栓塞可能是由心房颤动以外的疾病引起的,如血栓性血小板减少性紫癜、主动脉弓动脉粥样硬化(胆固醇栓塞)、感染性心内膜炎、非细菌性血栓性心内膜炎、心脏肿瘤或心肌病。但患者血小板计数正常,血培养阴性,超声心动图未见异常,无全身感染症状。考虑到潜在癌症的可能性,非细菌性血栓性心内膜炎仍有可能发生。然而,这种情况导致较大的多灶性梗死,这可能是由于潜在癌症相关的高凝性和易碎的瓣膜增生物相关的栓塞负担6。
大动脉粥样硬化
该患者有几个动脉粥样硬化的危险因素:年龄较大、未经治疗的心房颤动、冠心病、慢性高血压、高血脂、糖尿病、吸烟、大麻使用和早发性冠心病家族史。影像学检查显示颅外、颅内动脉有动脉粥样硬化,并有白质病变,这并不奇怪,可能是慢性微血管缺血所致。然而,他在4周内频繁发作,这不是动脉粥样硬化引起卒中的典型特点,特别是在使用抗血小板药物和抗凝剂治疗的情况下7。潜在的动脉粥样硬化和慢性微血管缺血可能降低了与其他机制相关卒中的阈值。
未确定原因和其他原因
此患者可能患有不明原因的隐源性栓塞性卒中。最近的研究阐明了这种情况的隐蔽原因,可以通过集中检测来确定8。
对于该患者,根据临床病情进展迅速、梗死分布特点以及CT血管造影未见非动脉粥样硬化性病变,可以缩小总体的鉴别诊断范围。重要的是要注意脑深部梗死的位置(如大脑脚和小钳[forceps minor])。来自中央栓塞源的栓子流(例如,未接受抗凝治疗的心房颤动患者左心耳的血栓)通常会进入远端皮质区域。与此相反,该患者梗死部位较深,动脉血栓形成是其卒中的原因。
小血管脑动脉病
诊断方法
该患者可能患有小血管性脑动脉病。小血管脑动脉疾病的鉴别诊断很广泛(表1)。具体动脉疾病的诊断依赖于以下因素,如患者的年龄、家族史、进展速度、系统性体征(如皮肤和视网膜病变)和脑外神经功能缺损(如神经病变)、脑和血管影像学检查观察到的特征以及诊断检查的结果(包括炎症和癌症生物标志物的检测),基因检测,脑脊液(CSF)分析,皮肤、颞动脉和脑活检9。

感染、炎症、辐射和药物
对于该患者,由于无发热、全身症状、皮肤病变和脑膜刺激征,因感染和风湿病导致小血管脑动脉病的可能性很低。然而,需要进行CSF分析和其他检查,以排除这些情况。辐射或药物引起的动脉病变可以排除,因为患者没有暴露于辐射或使用血管收缩药物的历史。虽然他吸过大麻,但大麻只有较弱的血管收缩特性,不太可能引起复发性多灶性梗死10。
单基因疾病
这名患者可能患有遗传性动脉疾病吗?脑常染色体显性动脉病伴皮质下梗死和脑白质病(CADASIL)患者,由19p染色体上的NOTCH3突变引起,可出现情绪障碍、偏头痛和小血管卒中11。预期MRI表现为小梗死灶和累及外囊和前颞叶的白质改变。由TREX1突变引起的伴有脑白质病和全身表现的视网膜血管病变(RVCL-S)患者可出现视力症状,视网膜和小的脑梗死,以及轻度肝功能和肾功能障碍12。CADASIL、RCVL-S和其他遗传性动脉病很罕见,在所有卒中患者中占比不到1%。此外,症状通常在患者25至50岁时出现,疾病进展速度比该患者要慢得多13。因此,不太可能是单基因动脉病。
原发性中枢神经系统血管炎
该患者的表现与原发性中枢神经系统血管炎(PACNS)一致,这是一种罕见的血管炎,局限于脑、脊髓和软脑膜的中小动脉和静脉14-16。PACNS最常发生在40至60岁的患者。男性发病率是女性的两倍。在该患者中观察到的急性至亚急性脑病和多灶性神经功能缺损与PACNS的诊断一致。该患者未报告头痛,而头痛很常见。
MRI显示的多灶性点状梗死是PACNS的典型表现。其他潜在的MRI表现包括弥漫性双侧半球白质高强度、软脑膜增强和类似肿瘤的肿块病变17。CSF分析显示蛋白水平升高,淋巴细胞增多。脑血管造影阳性时显示多灶性非同心圆动脉不规则,通常在远端分支。然而,由于PACNS主要影响无法显像的小口径动脉,因此脑血管造影诊断PACNS的敏感度仅为10%~20%。颅内血管壁MRI可显示血管壁呈同心圆样增厚和增强,这些特征可将PACNS与其他炎症性或非炎症性动脉疾病区分开来。然而,PACNS的明确诊断需要脑活检18。
PACNS的临床病程通常是进展性的19。治疗策略包括糖皮质激素诱导治疗和静脉给予环磷酰胺,随后给予免疫调节剂维持治疗,如口服环磷酰胺、硫唑嘌呤、吗替麦考酚酯、利妥昔单抗或甲氨蝶呤。PACNS的一个重要类似疾病是中枢神经系统(CNS)血管内淋巴瘤;需要进行CSF恶性细胞分析和脑活检来排除这一疾病。
副肿瘤性血管炎
虽然PACNS是该例患者的可能诊断,但胸部和腹部影像学检查结果表明患者可能罹患癌症。多达10%的卒中患者被确诊为肺癌、胃肠癌和其他癌症,在约5%的病例中,卒中是癌症的首发表现20。癌症相关卒中的常见机制包括高凝和非细菌性(消耗性)血栓性心内膜炎,后者通常导致多灶性、广泛分布的大小不等的梗死6。在极少数情况下,类似于PACNS的副肿瘤性血管炎可由以下机制之一引起:对血管内皮的免疫应答(分子模拟),肿瘤细胞释放促炎细胞因子导致内皮损伤,或对血管壁上沉积的肿瘤蛋白或含有肿瘤抗原的循环免疫复合物过敏21,22。
总结
该患者极有可能在肺癌背景下因副肿瘤性脑血管炎而发生多灶性小血管栓塞性卒中。我认为,除了肺、肾和脑活检,诊断检查还应包括CSF分析和颅内血管壁MRI作为辅助检查,以评估CNS血管炎,并排除类似这种情况的其他诊断。
临床印象
Silverman医师:虽然接受了抗凝治疗,患者仍出现多次复发性卒中。根据皮质下脑梗死和进行性脑白质病变,我们怀疑小血管病变。更具体地说,考虑到他的肺部和肾脏肿块,怀疑是与潜在癌症相关的小血管炎。下一步的诊断检查包括颅内血管壁MRI、CSF分析以及肺部和肾脏肿块的活检。
临床诊断
复发性皮质下梗死伴进展性白质脑病
Aneesh B. Singhal医师的诊断
肺癌背景下中枢神经系统副肿瘤性血管炎引起的多灶性血栓性脑梗死。
影像学检查
Romero医师:高分辨率、造影剂增强的血管壁MRI是一种相对较新的影像学检查技术。此方法突出显示动脉和静脉血管壁的特征,如炎症、血管壁增厚、出血和钙化。在该患者中,颅内血管壁MRI(图2)显示双侧颈内动脉和大脑中动脉的节段性同心圆样强化,可能提示非特异性炎症过程,如原因不明的血管炎。
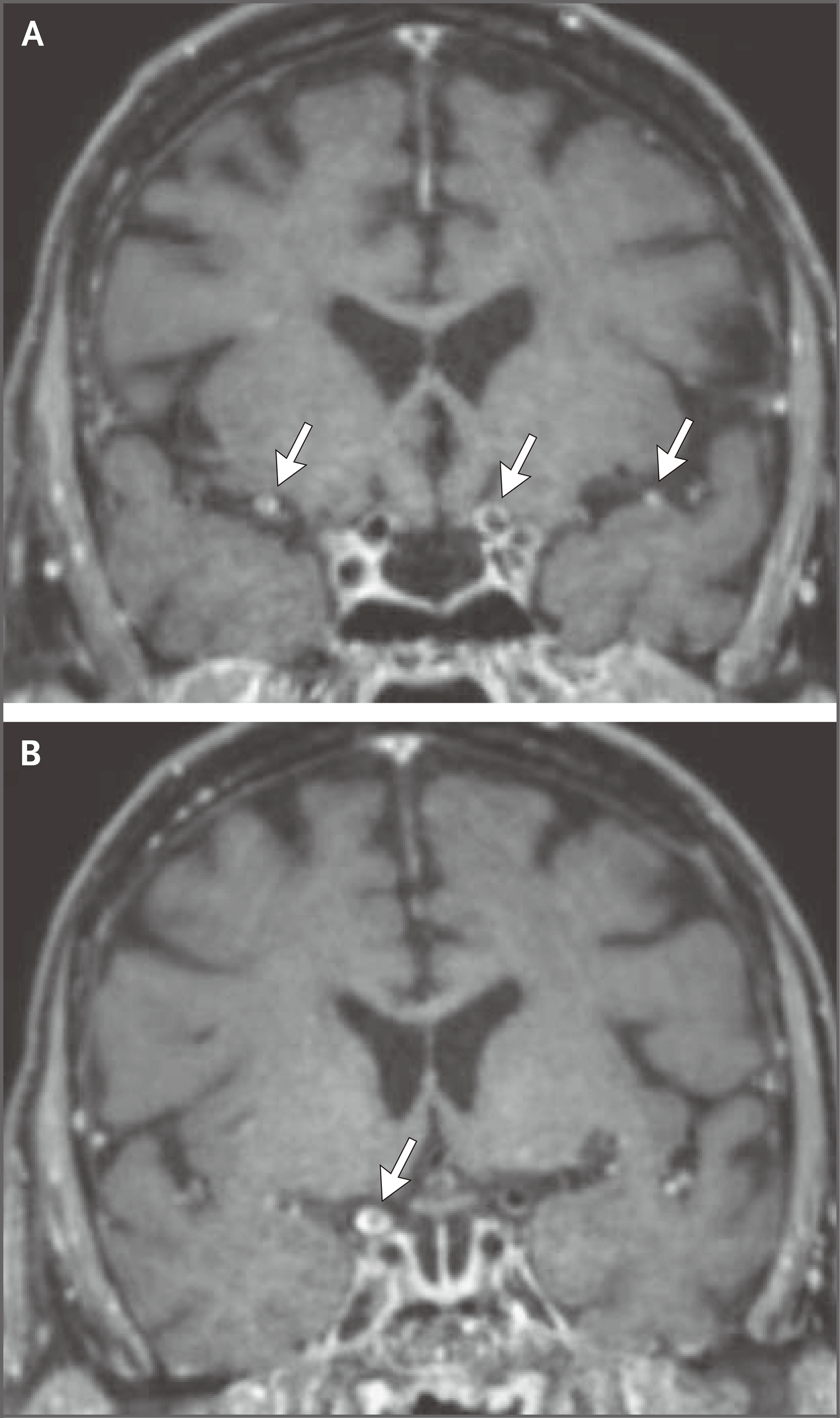
患者接受了高分辨率、造影剂增强血管壁MRI检查。冠状位图像显示双侧大脑中动脉M1节段(图A,箭号)和右侧颈动脉终点(图B,箭号)的同心圆样强化。
诊断检查
Melanie Lang-Orsini医师:CSF分析显示葡萄糖水平正常(50 mg/dL;参考范围,5~55),蛋白水平轻度升高(80 mg/dL;参考范围,50~75),有核细胞计数31个(97%为淋巴细胞)。微生物学检查结果为阴性。
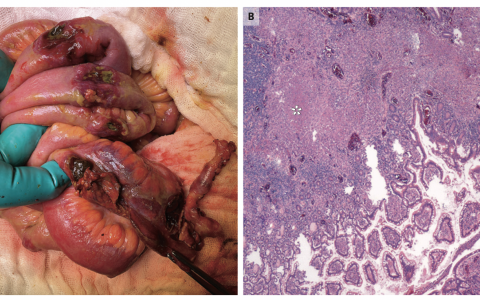
肺肿块和纵隔淋巴结空芯针活检标本(图3A和3B)显示为不典型细胞簇样腺癌,细胞核增大且不规则,细胞质稀少。肿瘤细胞TTF1免疫组化呈阳性;这一发现与原发性肺腺癌一致。肾脏肿块的活检标本(图3C、3D和3E)显示淡色多边形细胞正在形成管状结构。肿瘤细胞PAX8阳性;这一发现与原发性肾肿瘤一致,而肺腺癌转移。肿瘤细胞表达AMACR和CD117。形态学特征和免疫表型符合低级别乳头状肾肿瘤,但需要鉴别是乳头状腺瘤还是乳头状肾细胞癌。为了区分这两种疾病,需要综合考虑病理检查结果需要与影像学检查结果。然而,总的来说,这种低级别病变不太可能是患者症状的原因。
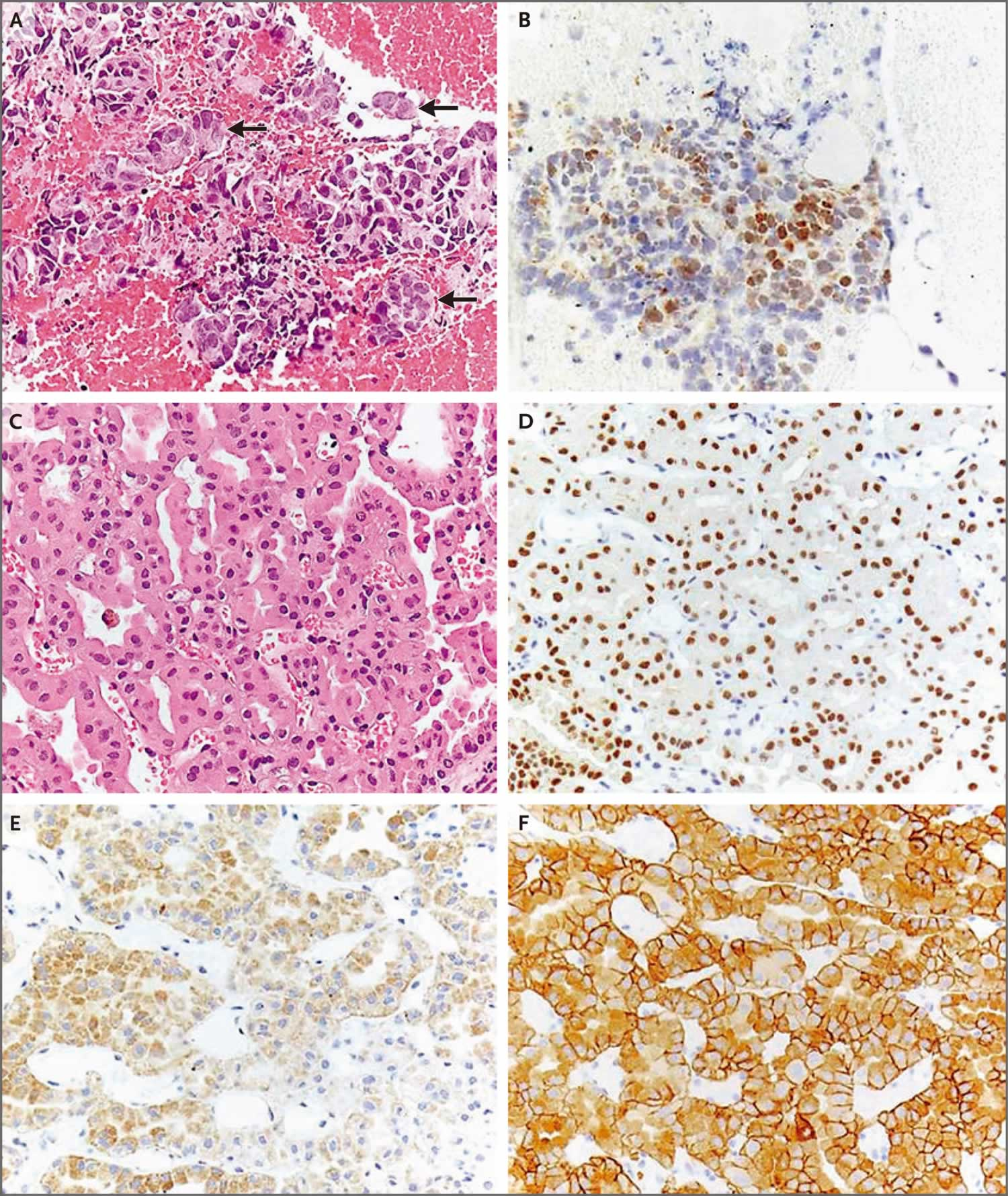
纵隔淋巴结空芯针活检标本。苏木素伊红染色显示转移性腺癌,由不典型细胞簇组成,细胞核增大不规则,细胞质稀少(A图,箭头)。免疫组化染色显示TTF1在肿瘤细胞核中表达(图B),与转移性肺腺癌一致。同时还获得了肾脏肿块的活检标本。苏木素伊红染色显示,淡色多边形细胞形成管状结构,细胞质呈粉红色颗粒状,细胞核为圆形(图C)。免疫组化染色显示细胞核表达PAX8(图D)、AMACR(图E)和CD117(图F)。
病理诊断
原发性肺腺癌合并纵隔淋巴结转移。
治疗讨论和随访
Silverman医师:CSF淋巴细胞增多和颅内血管壁MRI结果与血管炎的诊断一致。结合肺活检的结果,这些结果与肺腺癌相关副肿瘤性CNS血管炎的临床诊断最为一致。由于我们高度怀疑癌症背景下的CNS血管炎,所以没有进行脑活检。
在请神经免疫学团队会诊后,我们对CNS血管炎进行了免疫抑制治疗。患者接受5天甲泼尼龙静脉给药,随后每日口服泼尼松。他接受了一剂环磷酰胺静脉给药,并计划进一步接受治疗。由于其心房颤动病史、新发现的癌症以及可能潜在高凝状态,患者继续进行抗凝治疗。患者在住院期间接受肝素静脉给药治疗。出院前,治疗过渡到依诺肝素,并测定凝血因子Ⅹa水平,以确认达到抗凝状态。由于有冠心病病史,患者继续接受小剂量阿司匹林治疗。在请肿瘤学和放射肿瘤学团队会诊后,我们计划对肺腺癌进行放疗,对低级别肾肿瘤近进行观察。
患者被转到一家康复医院。四天后,他因低氧血症入住本院。胸部CT显示左肺下叶肺栓塞和肿瘤增大。开始静脉输入肝素治疗。患者有大量咯血、低氧血症型呼吸衰竭和低血压,需要使用血管加压药以进行血流动力学支持治疗。在征询患者医疗代理人的意见后,治疗目标转变为姑息治疗,患者在医院去世。进行了尸检。
尸检
Lang-Orsini医师:尸检时,脑重1470 g,有多处梗死,主要在白质内。这些梗死既有由巨噬细胞簇组成的亚急性梗死(图4A),也有较陈旧的梗死(空腔含有巨噬细胞,周围环绕着反应性神经胶质细胞增生)(图4B)。在梗死相关区域和梗死无关区域,可见散在分布的血管周围和血管壁内淋巴细胞浸润(图4C)。CD3和CD20免疫组化染色显示,淋巴细胞以T细胞为主(图4D),并有散在的B细胞(图4E)。CD68染色显示散在的血管周围巨噬细胞,梗死灶内也有突出显示的巨噬细胞(图4F)。不同阶段的多灶性梗死结合血管周围T细胞浸润与经过治疗的血管炎最一致。
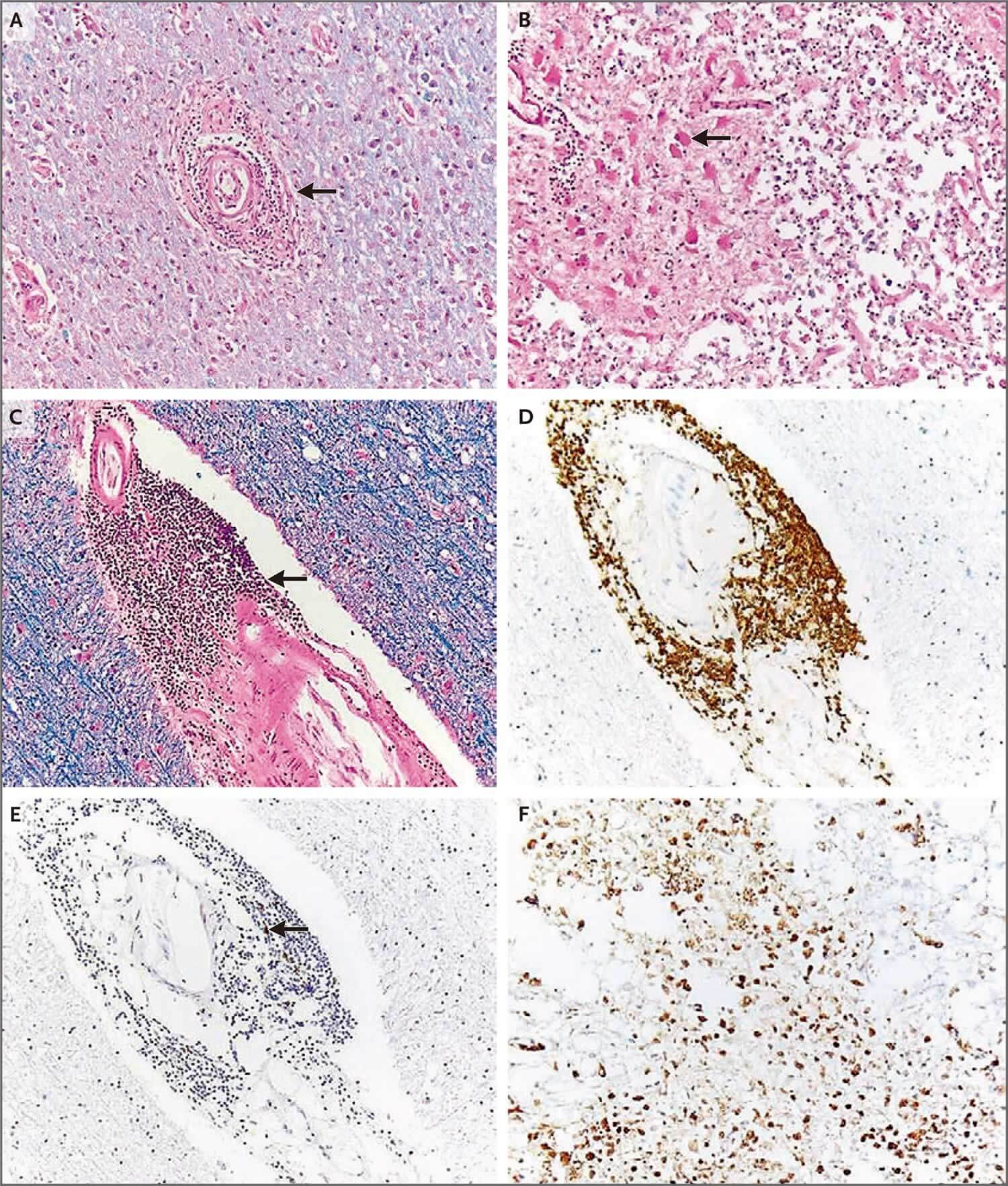
苏木素伊红染色显示脑内多灶性梗死。亚急性梗死由大片的巨噬细胞组成,中心有血管壁被淋巴细胞浸润的小动脉(图A,箭号)。亚急性至陈旧性梗死由一个包含巨噬细胞的空腔和一圈反应性星形胶质细胞组成(图B,箭号)。小动脉壁有密集淋巴细胞浸润,与梗死无关(图C,箭号)。CD3和CD20免疫组化染色显示,淋巴细胞以CD3+ T细胞为主(图D),并有散在的B细胞(图E,箭号)。CD68染色突出显示梗死区内的巨噬细胞(图F)。
血管炎不能进一步分类,因为之前用糖皮质激素治疗可以改变其外观。然而,PACNS往往肉芽肿性更强,巨细胞动脉炎可能与软脑膜或大脑皮层的大口径肌性动脉炎症相关。此外,没有证据表明转移癌累及CNS。
肺部病理检查证实诊断为累及两个左肺门淋巴结的腺癌。左肾检查发现边界清楚的结节(直径1.5 cm),符合低级别乳头状肾肿瘤,最符合乳头状腺瘤。
Silverman医师:尸检结果与CNS血管炎一致,并伴有治疗相关的变化。虽然糖皮质激素治疗限制了进一步的分类,但在病理检查中未发现PACNS或全身性血管炎的典型特征。新诊断的肺癌与小血管炎引起的复发性卒中相关,使得副肿瘤病因成为最可能的诊断。
最终诊断
中枢神经系统副肿瘤性血管炎。
作者信息
Aneesh B. Singhal, M.D., M.B., B.S., Scott B. Silverman, M.D., Javier M. Romero, M.D., and Melanie Lang-Orsini, M.D.
From the Departments of Neurology (A.B.S., S.B.S.), Radiology (J.M.R.), and Pathology (M.L.-O.), Massachusetts General Hospital, and the Departments of Neurology (A.B.S., S.B.S.), Radiology (J.M.R.), and Pathology (M.L.-O.), Harvard Medical School — both in Boston.
参考文献
- 1. Adams HP Jr, Bendixen BH, Kappelle LJ, et al. Classification of subtype of acute ischemic stroke. Definitions for use in a multicenter clinical trial. TOAST. Trial of Org 10172 in acute stroke treatment. Stroke 1993;24:35-41.
- 2. Ay H, Benner T, Arsava EM, et al. A computerized algorithm for etiologic classification of ischemic stroke: the Causative Classification of Stroke System. Stroke 2007;38:2979-2984.
- 3. Fisher CM. Lacunar strokes and infarcts: a review. Neurology 1982;32:871-876.
- 4. Topcuoglu MA, Saka E, Silverman SB, Schwamm LH, Singhal AB. Recrudescence of deficits after stroke: clinical and imaging phenotype, triggers, and risk factors. JAMA Neurol 2017;74:1048-1055.
- 5. Bamford J, Sandercock P, Dennis M, Burn J, Warlow C. Classification and natural history of clinically identifiable subtypes of cerebral infarction. Lancet 1991;337:1521-1526.
- 6. Singhal AB, Topcuoglu MA, Buonanno FS. Acute ischemic stroke patterns in infective and nonbacterial thrombotic endocarditis: a diffusion-weighted magnetic resonance imaging study. Stroke 2002;33:1267-1273.
- 7. Turan TN, Zaidat OO, Gronseth GS, et al. Stroke prevention in symptomatic large artery intracranial atherosclerosis practice advisory: report of the AAN guideline subcommittee. Neurology 2022;98:486-498.
- 8. Kamel H, Merkler AE, Iadecola C, Gupta A, Navi BB. Tailoring the approach to embolic stroke of undetermined source: a review. JAMA Neurol 2019;76:855-861.
- 9. Singhal AB. Diagnostic challenges in RCVS, PACNS, and other cerebral arteriopathies. Cephalalgia 2011;31:1067-1070.
- 10. Choi S-H, Mou Y, Silva AC. Cannabis and cannabinoid biology in stroke. Stroke 2019;50:2640-2645.
- 11. Chabriat H, Joutel A, Dichgans M, Tournier-Lasserve E, Bousser M-G. Cadasil. Lancet Neurol 2009;8:643-653.
- 12. Stam AH, Kothari PH, Shaikh A, et al. Retinal vasculopathy with cerebral leukoencephalopathy and systemic manifestations. Brain 2016;139:2909-2922.
- 13. Guey S, Lesnik Oberstein SAJ, Tournier-Lasserve E, Chabriat H. Hereditary cerebral small vessel diseases and stroke: a guide for diagnosis and management. Stroke 2021;52:3025-3032.
- 14. Hajj-Ali RA, Singhal AB, Benseler S, Molloy E, Calabrese LH. Primary angiitis of the CNS. Lancet Neurol 2011;10:561-572.
- 15. Salvarani C, Brown RD Jr, Christianson T, et al. An update of the Mayo Clinic cohort of patients with adult primary central nervous system vasculitis: description of 163 patients. Medicine (Baltimore) 2015;94:e738-e738.
- 16. de Boysson H, Zuber M, Naggara O, et al. Primary angiitis of the central nervous system: description of the first fifty-two adults enrolled in the French cohort of patients with primary vasculitis of the central nervous system. Arthritis Rheumatol 2014;66:1315-1326.
- 17. Singhal AB, Topcuoglu MA, Fok JW, et al. Reversible cerebral vasoconstriction syndromes and primary angiitis of the central nervous system: clinical, imaging, and angiographic comparison. Ann Neurol 2016;79:882-894.
- 18. Lehman VT, Brinjikji W, Kallmes DF, et al. Clinical interpretation of high-resolution vessel wall MRI of intracranial arterial diseases. Br J Radiol 2016;89:20160496-20160496.
- 19. Salvarani C, Brown RD Jr, Christianson TJH, Huston J III, Giannini C, Hunder GG. Long-term remission, relapses and maintenance therapy in adult primary central nervous system vasculitis: a single-center 35-year experience. Autoimmun Rev 2020;19:102497-102497.
- 20. Navi BB, Iadecola C. Ischemic stroke in cancer patients: a review of an underappreciated pathology. Ann Neurol 2018;83:873-883.
- 21. Taccone FS, Salmon I, Marechal R, Blecic SA. Paraneoplastic vasculitis of central nervous system presenting as recurrent cryptogenic stroke. Int J Clin Oncol 2007;12:155-159.
- 22. Patil A, Shree R, Naheed D, et al. Pearls & Oy-sters: paraneoplastic cerebral vasculitis: rare cause of spontaneous convexity subarachnoid hemorrhage. Neurology 2018;90(9):e815-e817.
特别申明:本文为转载文章,转载自NEJM医学前沿,不代表贪吃的夜猫子立场,如若转载,请注明出处:https://www.nejmqianyan.cn/article-info?permalinks=YXQYcpc2211368

 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫 
![[NEJM临床医学影像]:皮肌炎的眶周水肿](https://zyicu.cn/wordpress/wp-content/uploads/2023/05/image-49-480x300.png)