声明:
本指南适用于所有患者群体在体外膜肺氧合(ECMO)时的液体和电解质管理,旨在用于教育,以建立医生和其他卫生专业人员在评估条件和管理接受体外生命支持(ECLS)/ECMO患者的治疗方面的知识,并阐述了被认为对ECLS/ECMO有用的和安全的做法,但这些不一定是共识建议。临床指南的目的是帮助临床医生对他们的患者做出明智的决定。但是,遵守指南并不能保证成功的结果。最终,医疗保健专业人员必须在与患者协商后,利用他们的临床判断、见闻和专业知识,根据具体情况做出自己对于治疗的决定。这些指南不能代替医生和其他卫生专业人员对特定患者诊断和治疗的判断。这些指南无意也不应被解释为制定一个治疗标准,或被视为涵盖了所有正确的治疗方法,或者排除了其他合理的旨在获得相同结果的治疗方法。最终判断必须由医生和其他卫生专业人员以及患者根据个体患者呈现的所有情况以及临床状况的已知变异性和生物学行为做出。这些指南反映了在指南制定时期的数据;后续研究的结果或其他信息可能会导致对这些指南中的建议进行审慎修订以反映新数据,但体外生命支持组织(ELSO)没有义务提供更新。在任何情况下,ELSO都不会对依赖这些指南提供的信息做出的任何决定或采取的行动负责。
关键词:急性肾损伤,新生儿,小儿,成人,体外膜肺氧合、液体超负荷、利尿剂,肾脏替代疗法
体外生命支持组织(ELSO)液体和电解质管理指南旨在为接受体外膜肺氧合(ECMO)支持的新生儿、小儿和成人患者的临床治疗提供共识。这些指南旨在补充第5版ELSO红皮书中概述的ECMO支持的建议。我们的小组代表一个国际ECMO临床医生小组,我们的目标是为急性肾损伤(AKI)、液体超负荷(FO)和包括使用利尿剂和肾脏替代疗法(RRT)在内的干预措施提供基于证据的方法。
新生儿和小儿体外膜肺氧合液体和电解质管理
液体超负荷(FO)
FO是ECMO的常见并发症[1-3]。FO在全球范围内被定义为液体正平衡,在新生儿和小儿群体中的定义缺乏严格阈值。美国重症医学学院将>10%的容量超负荷定义为关键阈值,在新生儿和小儿感染性休克中起关键作用[4]。相同的>10%FO阈值与多种不良结果独立相关,包括ECMO持续时间的增加以及新生儿和小儿患者的死亡率增加[1-3]。在ECMO支持的患者中,FO与氧合受损、ECMO持续时间延长和死亡率相关[2]。重要的是,一旦确定将FO纠正至≤10%与提高生存率无关,这强调了预防和早期积极的液体管理策略的重要性[2]。传统上,液体平衡方法是通过测量液体输入和输出量来评估FO,已被用于计算FO百分比。然而,准确的液体摄入量和输出量可能难以量化,特别是在新生儿和儿童中有使用尿布量化输出量的患者。为了更好地量化准确的输出量,可以使用导尿管。然而,必须考虑长期放置导尿管导致尿路感染的风险。每日体重已被用作FO的替代指标,基于体重的FO测定与液体平衡方法高度相关,在儿科重症监护病房患者中具有相似的预测能力[5]。然而,Goldstein等人6建立了用于确定危重儿童FO的最常用方法如下:

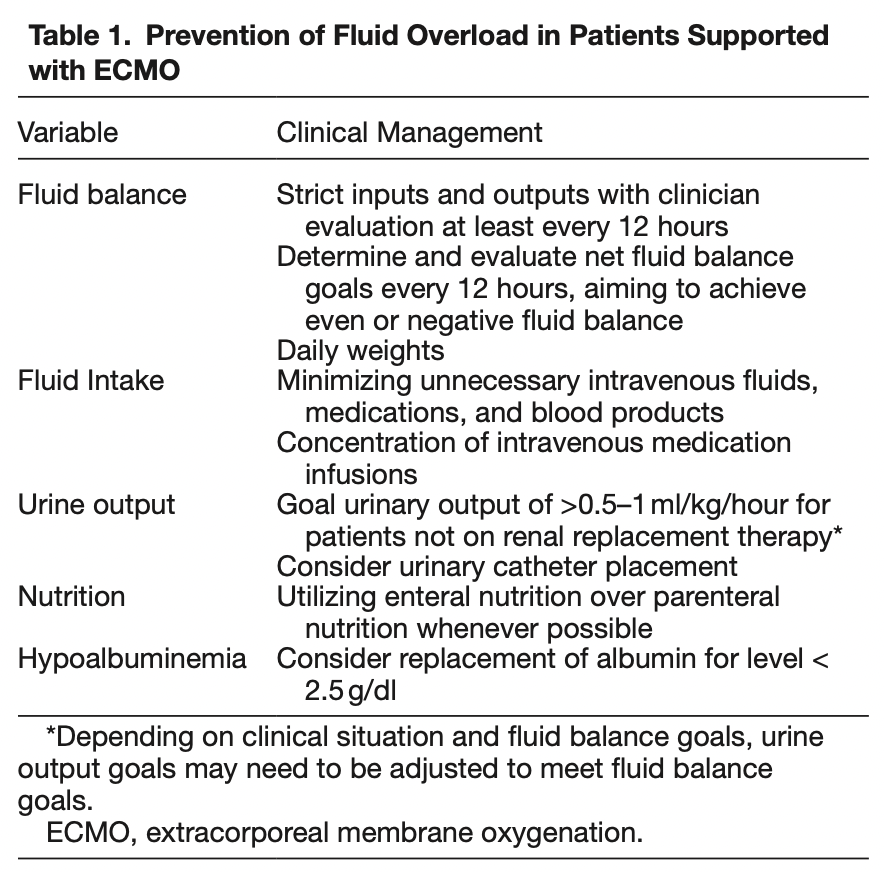
同样,由于将FO纠正至≤10%与提高生存率无关,因此预防FO>10%至关重要。表1列出了将ECMO支持患者的FO最小化的管理策略。
急性肾损伤病因学
AKI是许多接受ECMO支持的新生儿和小儿患者所经历的另一种常见并发症[7,8]。ECMO期间AKI的原因是多方面的。AKI可能与源自体外治疗本身或与体外治疗相关的几种疾病有关。在开始ECMO之前,这些患者经常出现败血症、缺血、心脏和/或呼吸衰竭、血流动力学不稳定、血管活性药物和肾毒性药物。所有这些因素都将患者置于AKI的高风险中[9]。其他促成因素包括通过与ECMO回路相互作用而激活的炎症级联反应,以及与ECMO直接相关的因素,例如红细胞应激和溶血。同时发生的其他器官衰竭和并发症包括神经系统事件、血栓形成、感染、出血和凝血障碍也可能导致肾损伤。开始ECMO并随后调整血管活性药物可导致快速的血流动力学波动,从而改变肾血流,导致再灌注损伤相关的AKI。ECMO之前和期间的FO会导致和恶化AKI[3]。
定义
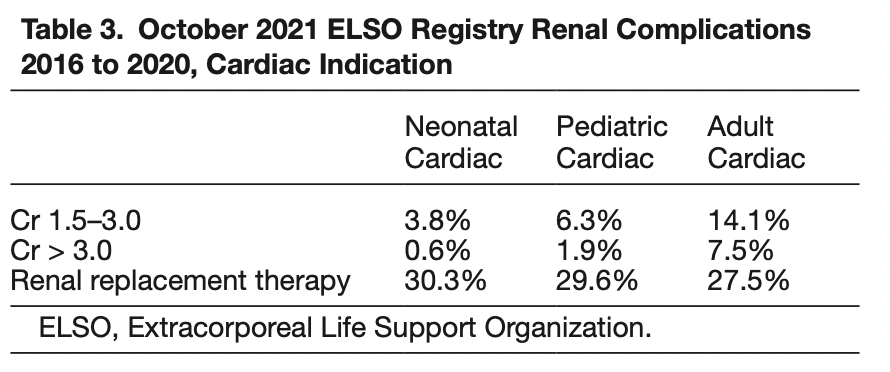
由于缺乏AKI的标准化定义,ECMO上报告的AKI发生率差异很大,介于30%和85%之间[10-12]。在KIDMO研究小组的一份出版物中,ECMO支持的新生儿和小儿患者发展为AKI,60%是用基线肌酐升高的定义,而74%的AKI是使用基线肌酐升高的定义和/或需要肾脏支持疗法[8]。ECMO期间的AKI与ECMO持续时间延长以及新生儿和小儿患者的死亡率独立相关[7,8]。在过去的 20 年中,文献中出现了多种AKI定义和分期系统,包括RIFLE(风险、损伤、衰竭、丢失、终末期肾病)、AKIN(急性肾损伤网络)以及最近的KDIGO(改善全球肾脏病预后组织) [13-15]。KDIGO是最现代的、专家认可的分期系统,可用于新生儿和小儿AKI的诊断和报告。在ELSO注册国际摘要中,肾脏并发症分为血清肌酐1.5–3.0mg/dL(0.13–0.27mmol/L)、肌酐>3.0mg/dL>0.27mmol/L)和需要肾脏替代治疗。报告的有肾脏并发症的ECMO运行百分比按年龄类别和适应症列于表2和3 [16]。

评估
一旦确诊,应进行详细病史和体格检查以确定AKI的根本原因,并建议多学科团队进行。ECMO本身是公认的新生儿和小儿AKI的危险因素,继发于脓毒症和心脏病等疾病过程的低灌注也是如此。应考虑通过尿液分析和肾脏超声以及肾血管多普勒检查进行初步评估,以排除先天性肾脏异常、梗阻性尿路病变和肾静脉血栓形成。提供者应评估并确保维持足够的平均动脉血压以灌注肾脏。肾脏近红外光谱(NIRS)可能是监测接受ECMO支持的新生儿和小儿患者的一种有用的非侵入性方法。由于FO非常常见并且与这些患者的死亡率增加相关,因此需要仔细和持续地评估容量状态,包括体重、生命体征以及液体摄入和输出。还需要对药物清单进行彻底审查,以确定并可能消除肾毒性药物,并且应酌情考虑使用非肾毒性药物。在AKI期间,连续监测电解质是必要的,包括高钾血症和低钠血症在内的电解质异常在危重儿童中很常见。
液体超负荷和急性肾损伤的处理
不幸的是,AKI的特定治疗药物有限,治疗主要是支持性的。新生儿和小儿ECMO期间FO和AKI的治疗选择包括液体限制、利尿剂和连续肾脏替代治疗 (CRRT)。间歇性呋塞米给药是许多机构的常见做法,连续输注呋塞米和布美他尼等利尿剂也是如此,但指导实践的数据很少。最近,研究人员开发了一种“呋塞米挑战试验”,使用单剂呋塞米挑战和评估肾小管完整性,单剂呋塞米后尿量减少预示进行性AKI[17]。在这种情况下,应该强烈考虑限制液体,而不是继续使用利尿剂,早期CRRT可能是必要的。在ECMO期间经常使用CRRT。在KIDMO研究小组的一份调查报告中,23%的受访者报告称在ECMO期间未使用CRRT。然而,大多数中心在ECMO期间使用CRRT 来治疗FO、AKI和电解质异常等适应症[18]。启动CRRT的时间仍然存在争议。由于新生儿和小儿ECMO期间对CRRT的需求与死亡率增加独立相关,因此提供者可能倾向于仅在面临压倒性FO或无尿时使用CRRT[7]。然而,早期开始CRRT可能会发挥作用,因为优化CRRT的时间和实施可以通过改善液体平衡管理对生存产生积极影响[2,3,19]。考虑到这一目标,一些中心对大多数ECMO患者使用早期CRRT。在最近的一份多中心报告中,早期CRRT的使用(定义为从ECMO第0天或第1天开始CRRT)与ECMO死亡率或住院死亡率无关[20]。
体外膜肺氧合肾脏替代治疗的适应症
目前,ECMO中心特定专家意见和经验推动了启动ECMO联合RRT治疗的决定。国际ELSO指南建议“将细胞外液量恢复到正常(干重)并维持在该水平。” [21]多项研究表明,早期RRT预防FO可能会改善预后并值得进一步研究。一些研究强调了累积FO及其与死亡率、住院时间和机械通气持续时间增加的关系[1,22-24]。累积FO和未能恢复干重与更高的死亡率和延长ECMO持续时间有关[5,25]。液体平衡的下降与肺功能的改善和ECMO支持的撤机时间有关[26]。
体外膜肺氧合肾脏替代治疗的技术考虑
ECMO期间的RRT选项包括腹膜透析、间歇性血液透析和CRRT。CRRT通常用于ICU,以提供有效的肾脏替代和液体管理方法,同时确保血流动力学稳定性。CRRT包含广泛的技术。基于膜渗透性、分子清除方法、治疗持续时间和使用的设备,存在几种模式。先前的研究表明,ECMO期间RRT的实践存在很大差异[18]。由于没有对这些技术进行比较研究,因此实践通常基于当地经验。在ECMO期间执行CRRT有三种主要方法:1)独立CRRT接入,2)在ECMO回路中引入导管内血滤器,以及 3)在ECMO回路中引入CRRT装置。
独立的肾脏替代疗法通路
RRT可以通过获得独立于ECMO回路的静脉通路来提供。然而,这需要在ECMO之前完成导管放置或尝试对抗凝ECMO患者放置血管通路。在需要ECMO的新生儿和小儿患者中,建立足够的血管通路通常具有挑战性。一旦患者建立了ECMO支持,体外回路就可以用作一个平台,在该平台上可以连接其他形式的器官支持,而不会使危重患者面临放置额外血管通路的风险。
将血滤器引入体外膜肺氧合回路(导管内血滤器)
将血滤器引入ECMO回路是一种用于提供CRRT [18]的技术,并且具有相对简单和便宜的优点。血滤器通常放置在泵之后以提供向前的血液流动,并在氧合器之前放置以捕获引入回路中的任何空气或凝块。通过血滤器和线路分流器的创建,测得的流量与输送给患者的流量(这表明血滤器的血流量)之间存在差异。超声流量探头应放置在ECMO回路的回输端上,以确定输送给患者的实际流量。
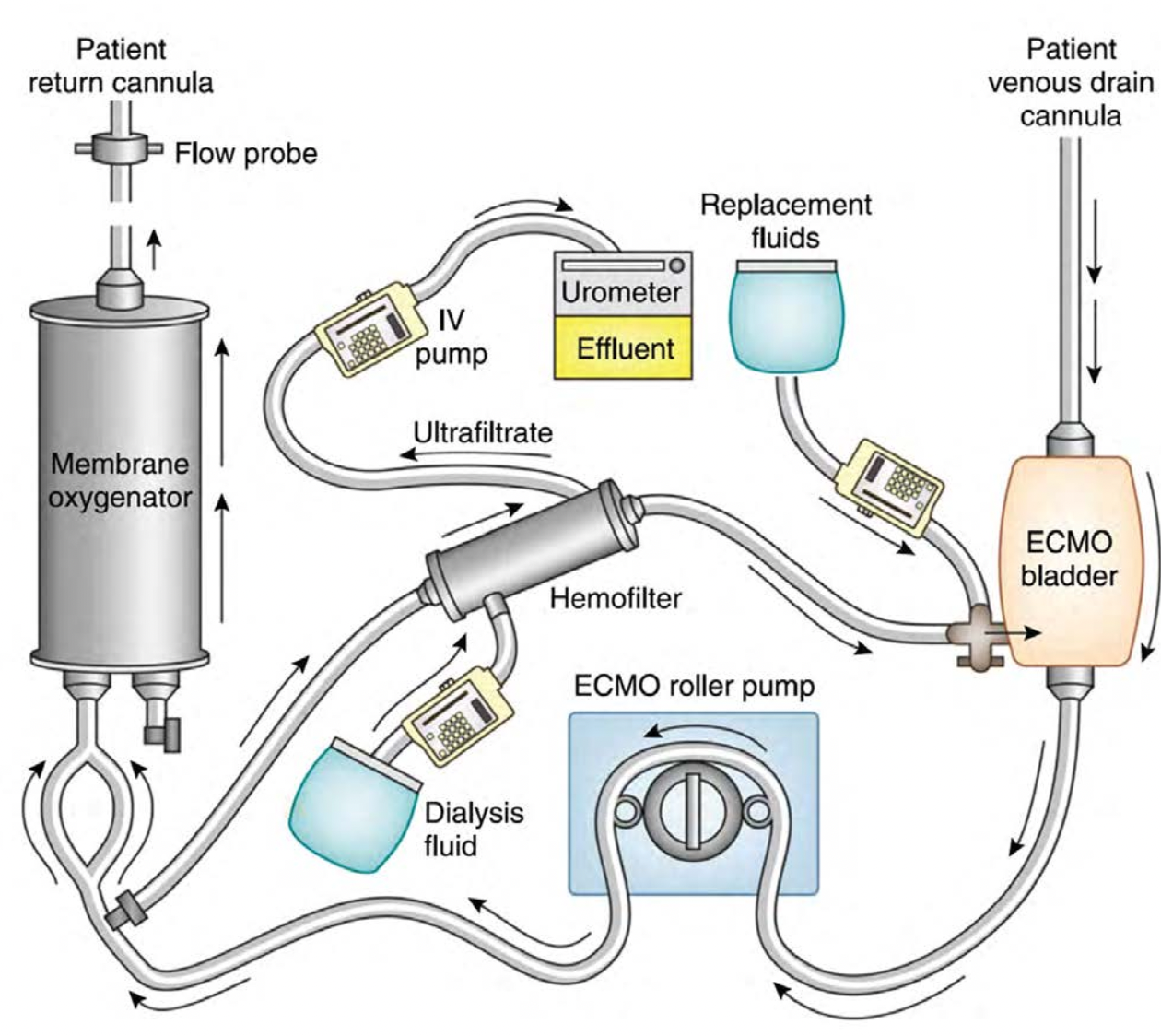
一些中心使用这种技术仅提供缓慢的连续超滤,而其他中心使用导管内血滤器与肾脏替代液或透析液结合使用(图1)。由于这些血滤器被设计用于高压系统,因此纤维特性使扩散清除比传统膜更有效。血滤器有可能产生大量超滤液,这通常需要使用连接到血滤器流出端口的标准静脉输液泵装置进行调节。这些静脉输液泵的最大流量通常约为1L/小时。与使用连接到ECMO回路的CRRT装置相比,使用导管内血滤器和静脉输液泵已被证明在ECMO期间提供的液体管理准确度较低[27]。有几种方法可以确定排出的液体量。通过重量或使用体积测量装置测量超滤液的实际体积是常见的。
将床边持续肾脏替代治疗装置引入体外膜肺氧合回路
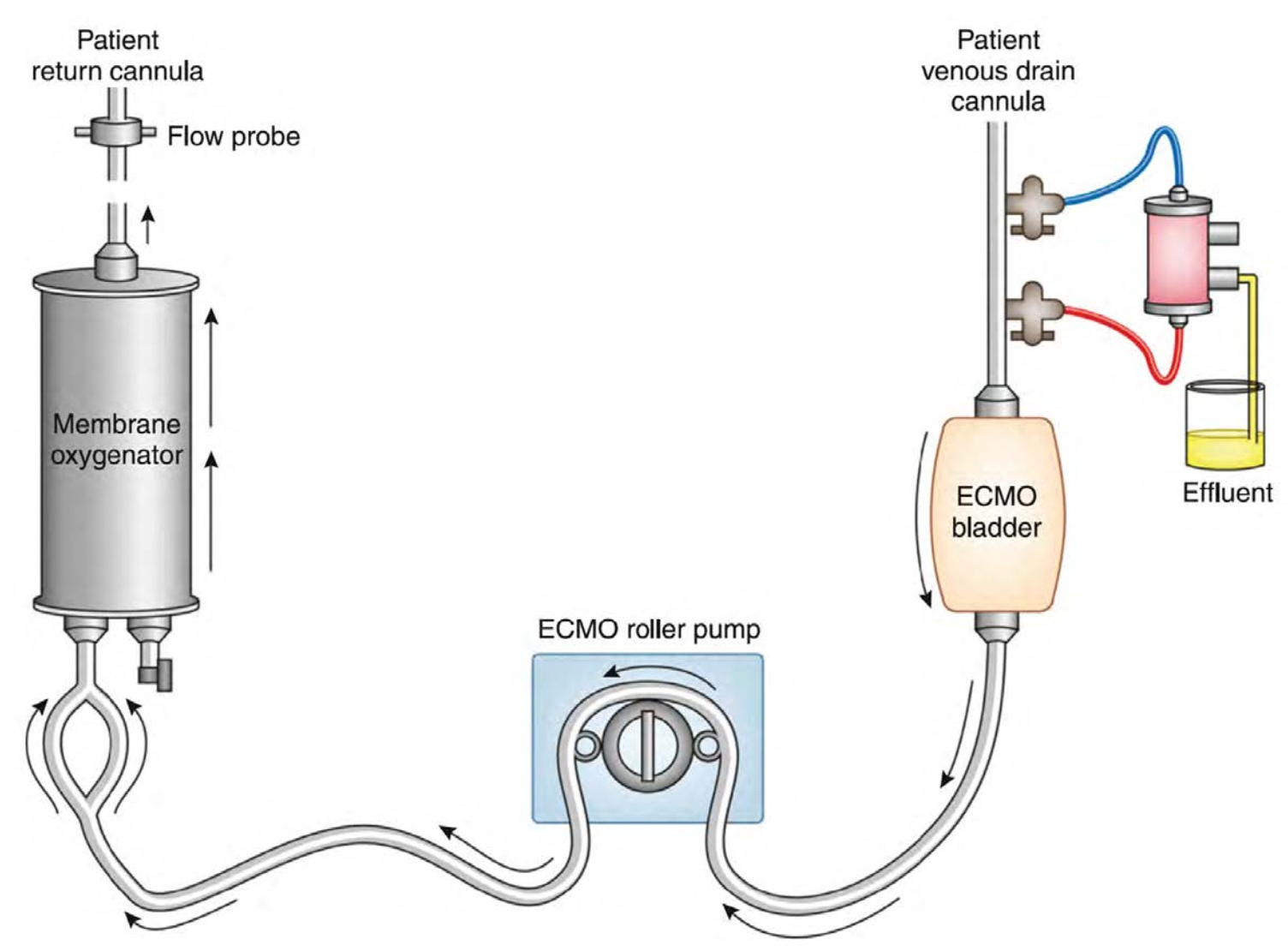
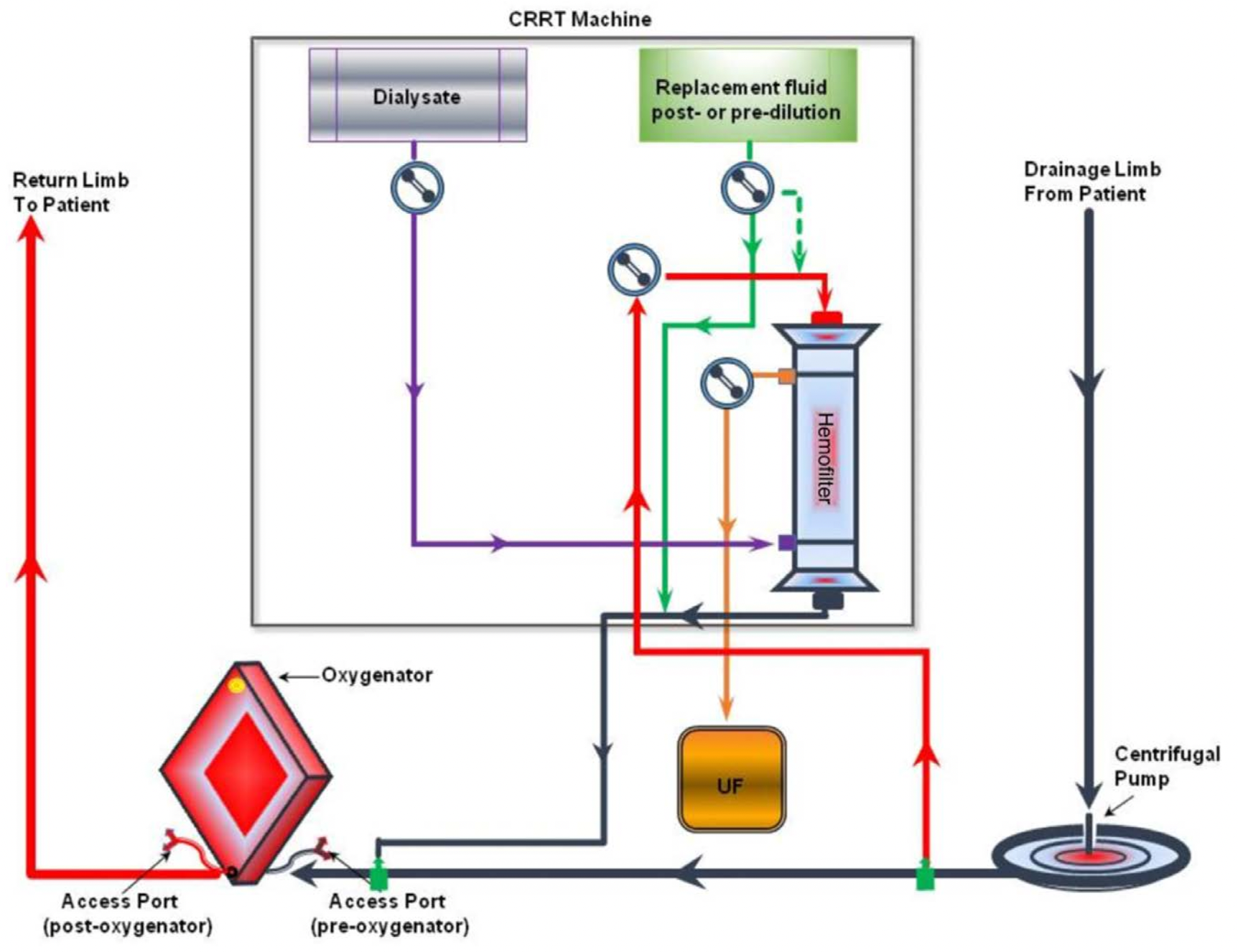
当ECMO设备使用滚轴泵时,可以将CRRT装置连接到ECMO回路泵前的静脉支(图2)。如果ECMO设备使用离心泵,最好在泵后连接CRRT设备,因为有将空气吸入ECMO回路的风险(图3)。无论ECMO设备使用哪种泵,建议将血液从CRRT设备返回到ECMO回路氧合器前,以确保如果有任何空气或血栓形成,是被送至氧合器,而不是直接返回到患者。与通过独立静脉通路进行CRRT相比,这种方法滤器寿命更长[28]。一些CRRT设备可使用软件实现正压接入或将接入报警限制调整到正范围,以方便CRRT与ECMO回路的同时在线使用。
体外膜氧合过程中持续肾脏替代治疗的长期影响
有关在儿童ECMO支持期间使用CRRT对肾脏的长期影响的资料很少。然而,一项大型单中心研究表明,在没有原发肾脏疾病的情况下,在新生儿和儿童ECMO支持期间使用CRRT后不会发生慢性肾脏疾病[29]。
成人体外膜氧合的液体及电解质管理
液体过负荷
ECMO支持的成人患者的补液和脱水非常常见。ECMO支持的成人危重患者发生液体过负荷的原因是多种多样的。可能会导致严重心肺功能衰竭的潜在疾病在初始复苏期间是需要大量的静脉输液的,需要输血和补液以维持足够的ECMO回路血流量。用于药物管理的液体也大大增加了日常的液体输入和液体正平衡。目前已经确定需要ECMO支持的患者发生急性肾功能损伤和液体过负荷后死亡率增高。使用利尿剂排出多余液体可达到液体平衡, CRRT可用于那些对利尿剂耐受或有明显肾衰竭的患者。
血管加压药和液体复苏的使用通常是由临床终点决定的,如维持平均动脉压大于60-65mmhg。血管内低血容量、ECMO循环管路抖动和高乳酸血症通常需要容量复苏。定期监测ECMO引流压力很重要,要注意负压越高,溶血越严重,应当避免。有观察性研究表明,体外膜肺氧合患者在第3天液体正平衡与低生存率相关[30-32]。日累积体液负平衡和更多的日平均体液负平衡均与行VV-ECMO和CRRT支持的成人患者的肺顺应性的改善密切相关[33]。
急性肾损伤和肾脏替代治疗
考虑到临床环境、患者分组、ECMO模式和定义急性肾功能损伤的诊断标准的不同,关于ECMO运转期间急性肾功能损伤发生比率的报道存在广泛的差异。使用 RIFLE定义的单中心研究表明,在ECMO支持的成人患者中,呼吸衰竭患者的急性肾损伤的发生率约为78%[12],在心内直视术后患者中为81%[34]。
ECMO支持患者行肾脏替代治疗的适应证和时机
液体过负荷和急性肾功能损伤是ECMO支持患者中行肾脏替代治疗的最常见的指征。肾脏替代治疗也被用于预防液体过负荷,调节电解质平衡紊乱,以及清除故意或意外摄入的内毒素。虽然单中心使用RIFLE, AKIN和KDIGO标准决定是否对成人急性肾功能损伤患者进行起始肾脏替代治疗,但肾脏替代治疗用于液体过负荷的标准则较为不统一,通常用于标准利尿疗法难以治疗的相对严重的急性肾功能损伤患者。CRRT的早期启动对需ECMO支持的新生儿患者的预后是有益的[35]。然而,目前在ECMO支持的成人患者中缺乏类似的数据。已经证实,发生急性肾损伤和脓毒性休克的成年患者,行早期肾脏替代治疗 (< 12小时)的患者与行延迟肾脏替代治疗(>48小时)的患者相比,90天死亡率没有显著差异[36]。作为一项指导原则,肾脏替代治疗应考虑在利尿治疗方案难治性的容量过负荷的ECMO支持的成人患者中,以及在急性肾损伤引起代谢紊乱、阻碍心肺功能恢复的情况下使用。
肾脏替代治疗回路的技术方面
ECMO期间可进行间歇透析、持续低效率透析(SLED)和CRRT的所有方式,包括:血液滤过、血液透析、血液透析滤过和超滤。肾脏替代治疗可以通过使用一个并行系统启动,其中一个单独的血管通路和回路将确保该过程不会干扰ECMO的血流量。然而,在抗凝患者中引入透析导管的风险始终存在,同时限制了额外ECMO置管的进入位置。串联的血液过滤器使用具有成本效益高,资源消耗少,而且设置简单等优点。将CRRT设备与ECMO回路相连,可以很好地控制液体平衡和清除溶质,优于串联血液过滤器。然而,这种连接需要完全了解ECMO回路压力,以确保CRRT安全运行。在ECMO离心泵之前,ECMO (-40 ~ -100mm Hg),而在泵和膜肺之间,ECMO回路压力为高正压,而CRRT机器被编程为在0-20mm Hg的低正压下工作。这可能会导致在回路中空气滞留和回路中血液湍流的报警。如前所述,在使用离心泵的ECMO回路中,强烈建议将CRRT设备连接在泵后,以防止空气滞留到回路中。CRRT设备的静脉端连接到膜肺前/泵后,以防止空气或血栓被输送至患者体内。
ECMO支持患者肾替代治疗剂量
肾脏替代治疗的剂量是根据逆流交换的速率或生理范围内含有葡萄糖和电解质的流出液的流速来确定的。然而,从重症医学文献中推断,对于体外膜肺氧合患者,一般推荐的标准溶质清除率为20 – 25ml/kg/h。肾脏替代治疗回路的血流量一般维持在100 – 250ml/min之间。对于间歇透析患者,透析方案是由肾内科医生或重症医学医师的评估决定的,采用的方案与其他危重患者类似。对于SLED,持续时间至少为6小时,血流速度为200ml/min,透析液速度为300ml/min。
体外膜氧合-肾替代治疗患者的肾脏修复
需要体外膜肺氧合和肾脏替代治疗的患者通常病情更重,死亡风险更高[37]。与ELSO中心登记相比,单中心研究的死亡率结果存在差异。尽管单中心研究报告需要同时进行肾脏替代治疗和ECMO支持的成人患者的死亡率大于75%,但根据ELSO国际注册报告显示,在ECMO期间需要肾脏替代治疗的成人呼吸疾病患者的生存率为49%,而心脏患者的生存率为32%[16]。此外,ECMO启动前3天行CRRT治疗是90天死亡率的独立预测因子[31]。在ECMO支持患者中需要透析的急性肾损伤患者比不需要透析的急性肾损伤患者预后更差[35, 39]。相比之下,在调整了其他研究中的混杂因素后,肾脏替代治疗对ICU死亡率的影响不显著[40]。在一项对ECMO支持的急性呼吸窘迫综合征患者的研究中,ECMO支持前需要肾脏替代治疗与死亡率增加独立相关,但ECMO支持期间需要肾脏替代治疗与死亡率增加无关[41]。最近发表的一项关于成人ECMO和肾脏替代治疗的研究证实,接受肾脏替代治疗7天的患者与接受肾脏替代治疗少于7天的患者具有相似的长期生存期。然而,在接受肾脏替代治疗7天的患者中,有较高的终末期肾病、呼吸机依赖和再入院率高的风险,这意味着慢性肾病和长期透析可能是那些需要更长时间的ECMO和 肾脏替代治疗支持的成人患者的后遗症[38]。
总结
ECMO被用于越来越多的患者和有越来越多的适应症。虽然每个ECMO中心都有自己的设备、经验和实践技术,但国际ELSO组织致力于提供一种实用的、以患者为中心的方法来解决急性肾损伤和液体过负荷的发病率和死亡率。
特别申明:本文为转载文章,转载自重症之声,不代表贪吃的夜猫子立场,如若转载,请注明出处:https://mp.weixin.qq.com/s/1w-CpVQAxId8IB7qruB69A

 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫