背景
动静脉-体外膜氧合(VA-ECMO)日益成为严重心肺功能衰竭患者挽救性的紧急生命支持手段[1, 2]。病死率降低及启动VA-ECMO的逐渐简易因而应用日益广泛[3]。
但相当一部分患者(30% – 70%)最终无法撤离VA-ECMO的支持,这至少部分掩盖了这些令人振奋的进步[4, 5]。如果患者并不具备植入心脏永久支持设备或是心脏移植的条件, 那么撤机失败毫无疑问意味着维持生命支持治疗的撤离。因此很明显在撤离VA-ECMO之前要重视并优化那些可逆的因素。自然在施行撤机试验前就应该明确这些阻碍成功撤机的相关因素。
据我们所知,这些因素并未从临床实践的角度完整系统的总结过。机械通气脱机困难患者熟知的“ABC”方法已经成为机械通气患者脱机流程的基础[6]。考虑到对于VA-ECMO患者的这种临床实践总结的迫切性,我们总结了VA-ECMO撤机失败的危险因素和基础疾病相关病因,为结构化的诊断和治疗手段提供日常工具。
VA-ECMO撤机失败
大量研究评估了VA-ECMO撤机失败的发生率及其危险因素[5]。但这些研究对撤机失败的定义大相径庭。部分作者认为撤机成功应定义为未(再次)置入其他的机械辅助设备下存活30天[5, 7, 8]。而其他团队则将临界时间窗限制在撤机后的48[9, 10]甚至是24小时[11, 12]。
仔细考量撤机成功的确切定义很重要,因为成功撤管并不肯定转化为患者预后获益[5, 13]。约有20%至60%的患者在撤管但在出院之前依旧死亡[4, 13]。这种所谓的ECMO缺口(ECMO gap)大多是因为持续的多器官衰竭,不良神经系统事件,出血,并发感染(主要为肺部感染)和失代偿性心功能衰竭[14]。还有10%的患者最终在出院后但在一年的随访期间死亡[15]。这可能主要是因为基础的疾病状态,以及在重症监护室长期住院后并发的获得性虚弱[16]。
VA-ECMO撤机失败的后果
对大部分患者而言VA-ECMO旨在作为通向恢复的桥梁。但当患者无法恢复而依赖于VA-ECMO时,患者预后不佳或需要长期的治疗[17]。唯一可能的处理是植入机械性循环辅助(mechanical circulatory support, MSC)设备如左心辅助设备(LVAD)或双心室辅助设备(BIVAD),或是紧急心脏移植。但这些桥接的治疗步骤通常限于那些有预后最佳的ECMO患者,并且患者的选择需要仔细评估并权衡特定的预后因素[18-20]。在法国,,VA-ECMO有优先心脏移植治疗资格,但在优化候补名单和移植后病死率期间,仍然需要体外支持12到16天[20]。
VA-ECMO撤离失败并最终接受LVAD治疗的患者的30天生存率为77%但在一年后跌至约50%[18]。该数据接近VA-ECMO支持治疗患者的总体生存率[15]。
VA-ECMO撤机失败ABC概念作为系统性手段
系统简明的评估所有的可逆性因素可最大程度的提高VA-ECMO支持患者的撤机的成功率,改善预后。由于每个个体患者都可能动态的涉及很多不同并潜在相互关联的因素,因此这个关键过程需要系统性的手段。在关于VA-ECMO撤机没有确切指南推荐且明确证据的情况下,本文的诊断和治疗性的推荐意见基于实践经验和作者观点,以及对于文献的严格评价。图1总结了各种相关因素。对于特定的案例可能有些因素更为重要。同时一些因素可能在ECMO支持的较早时期就已经评估过。本文所阐述的实践性手段旨在完整总结引起持续VA-ECMO依赖的因素。很自然这种手段也能用于推断那些撤管后临床恶化的患者。
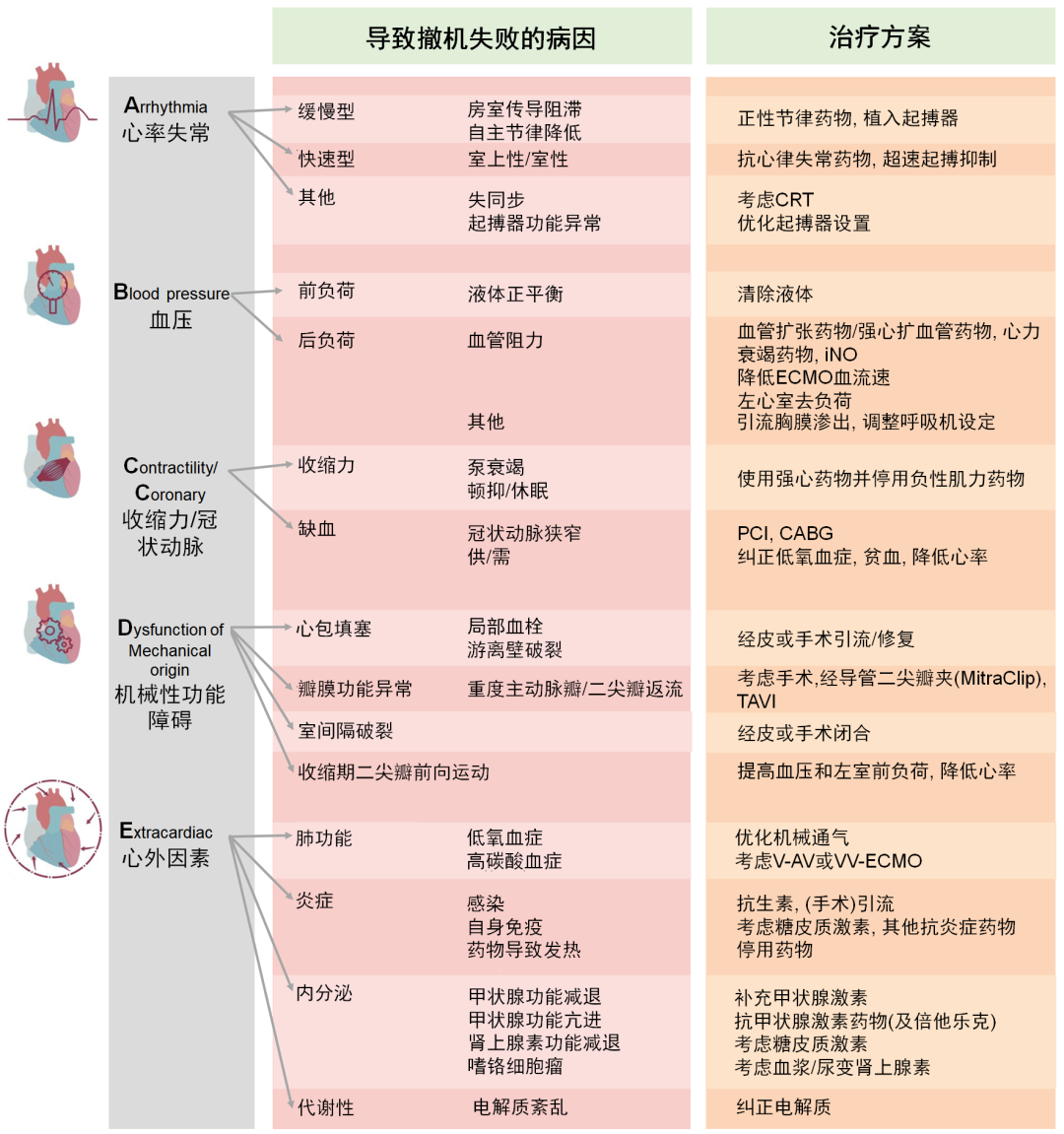
A: 心律失常(arrhythmias)
缓慢型和快速型心律失常都会引起心输出量的显著下降。因此建议VA-ECMO撤机时应尽量努力维持正常的窦性传导节律,心率在60 – 100次/分(bpm)。
缓慢型心律失常
理论上而言,VA-ECMO支持期间尽可能放缓心率有利于心力衰竭的恢复,可直接降低心肌的机械负荷,钙离子调控(异常)和过负荷及代谢需求。撤离VA-ECMO时有时可以接受窦性心律,心率60 – 80 bpm,特别是对于缺血性心脏病的患者。当心率降低本身严重影响心输出量,比如在相对不依赖于心率,“固定的”每搏输出量的情况下,则需要考虑使用临时起搏器设定在高的正常心率(100bpm)下以利于撤离VA-ECMO。这种情况下肾上腺素能药物可刺激心率的改变。从而可反应为高度房室传导阻滞,而远端传导阻滞也可能进一步恶化,也会需要临时起搏。
快速型心律失常
快心率(> 100 bpm)和心肌机械和代谢负担显著增加密切相关,因此需要尽可能的降低(特别是对于恢复期的心脏), 直至能够依然维持可接受的自然状态下的心输出量。
室上性(快速型)心律失常,如心房颤动和心房扑动在危重症中很常见,可由多器官衰竭时心血管功能衰竭和全身炎症综合导致[21]。(快速型)心律失常诱导的心肌病可引起严重的心源性休克需要VA-ECMO支持[22],但也可能导致持续性VA-ECMO依赖。心房收缩(arterial kick, 指在收缩期心房产生的力量增强的现象. 发生在心房收缩末期, 血流从左心房流向左心室. 心房收缩的目的在于增加压力梯度, 增加通过二尖瓣的血流. 在健康人中心房收缩占到流入左心室血流量的20%至30%, 听诊时为第四心音)的消失也会阻碍心室被动充盈并降低心室收缩力. 优先选择“节律控制(rhythm control)”的策略保证持续的“心房收缩”. 恢复窦性心律并不一定会立即恢复机械收缩力, 心房顿抑可维持数天. 因此当无法维持窦性心律时, 使用“心率控制”的策略同样有效[22]. 心律失常诱导的心肌病也表明严格的心率控制策略, 包括确切的房室结消融和心脏起搏的有效性[22].
多种因素均能引起VA-ECMO期间的室性心律失常, 包括电解质紊乱(参见“E: 心外因素”), 药物促心律失常的不良反应, 心肌缺血, 新出现的结构异常或是并发症(参见D: 机械性功能障碍). 出现心室心律失常时需要彻底的诊断性检查. 虽然室性心律失常并不会立即引起体外支持患者的血流动力学不稳定, 但生理心脏射血的消失会导致肺缺血, 左心淤血和扩张, 肺水肿和血栓栓塞事件, 因此需要立即处理. 根据涉及的基础的引起心律失常的机制, 植入临时起搏器并将心率设定在可出现室性心律失常的基础心率之上, 联合抗心律失常药物, 可预防其再次发生. 也可考虑导管消融术, 这在VA-ECMO支持时可安全操作[23].
失同步
心房-心室和心室间的失同步能显著影响心衰的严重程度和心输出量, 这已得到了广泛的认识. 而通过心房-心室和双心室起搏的再同步能改善心输出量和效率[24]. 从机制的角度而言, 使用永久起搏器优化心力衰竭也能为急性心力衰竭和VA-ECMO支持的患者带来益处. 但是目前鲜少有关于最佳的心房-室及双心室起搏的文献, 仅限于病例报道或是系列病例, 需要进一步的研究[25].
对于A: 心律失常的诊断和治疗推荐
- 1、尽力维持窦性节律. 当心输出量依赖于非常低的每搏输出量时, 考虑使用药物或是起搏达到约100次/分的心率.
- 2、积极纠正室性心律失常, 寻找相关促进因素.
- 3、对于影响心输出量的严重失同步, 考虑再同步治疗以利于撤机.
B: 血压和负荷状况
心衰管理的一个重要方面是降低前负荷和后负荷, 降低心肌代谢和氧需求, 缓解重构的进程从而减轻心肌的负担, 同时维持心脏完整功能. 这个重要概念可以直接转化为最佳血压的管理, 这在VA-ECMO中尤为重要, 因为此时的心脏还有额外的非生理性的来自体外循环管路的持续性主动脉逆向血流形成的负担[26, 27]. 虽然有这些挑战, 通过优化心室的前负荷和后负荷才能满足撤机最佳的先决条件.
许多因素都能够影响前负荷和后负荷, 其中一部分能够同时影响左心室(LV)和右心室(RV)[27, 28]. 这些因素总结见图2. 减少循环血量可以同时降低左右心室的前负荷. 左心室的后负荷主要由动脉血压所决定, 而这很大程度受全身血管张力和VA-ECMO血流的影响. 降低ECMO的泵速, 使用强心扩血管药物(inodilator)或是心力衰竭的药物从而降低ECMO的血流速和血压能改善左心室-心房耦合. 主动脉瓣开放不彻底甚至不开放; 心脏超声探测“冒烟”现象也反映左心室, 左心房或是降主动脉的血流降低; 肺毛细血管楔压(PCWP)或左心房压力显著升高(> 15 mmHg)或是出现肺水肿时, 均应当考虑辅助左心室去负荷. 注意在这种情况下左心房或是心室的扩张仅代表心脏的几何结构, 如果不考虑室腔压力并不一定解释为心肌过负荷.
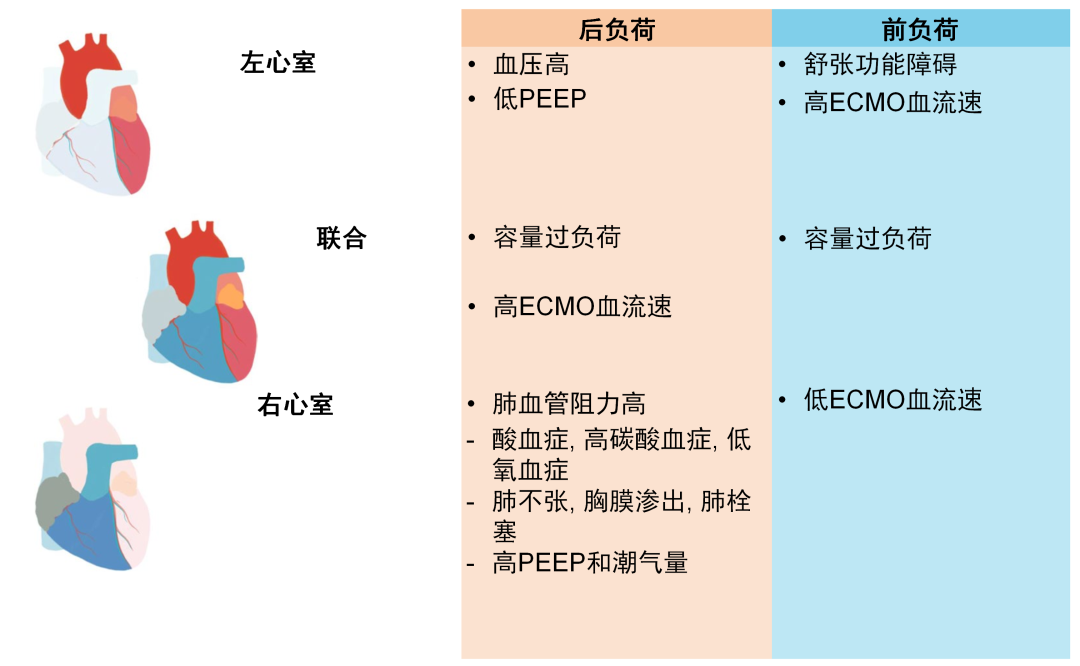
VA-ECMO支持时右心室一般都能够去负荷, 这也使其合适的收缩表现的评估更具挑战. 因此右心房-肺动脉耦合需要更大的关注, 因为右心室功能不全通常会成为VA-ECMO撤离过程中的限制性步骤. 尽力维持正常低限的动脉CO2分压和正常高限的动脉氧分压都能促进血管扩张, 从而优化肺血管阻力(PVR). 同时吸入一氧化氮(iNO)或是其他强效及选择性的动脉扩张药物也有助于显著降低PVR.
对于B: 血压和负荷状况的诊断和治疗推荐
- 1、使用强心扩血管药物, 可能的话使用治疗心力衰竭药物及降低ECMO的泵速, 在生理可耐受的前提下尽量降低后负荷.
- 2、对于右心室去负荷, 考虑目标为生理性pH或轻度碱中毒, 正常动脉二氧化碳和氧分压, 并考虑加用吸入NO.
- 3、对于左心室去负荷: a) 在终末脏器灌注能耐受的前提下尽量降低血压和ECMO血流速, 以及b) 考虑辅助性左心室去负荷.
- 4、在生理性可耐受的前提下, 使用利尿剂或是持续性肾替代治疗/超滤降低循环血量, 从而降低前负荷. 努力维持CVP < 12及PCWP < 15 mmHg.
C: 收缩力和冠状动脉
足够程度的收缩储备及在适当刺激下能够满足循环需求是成功撤离VA-ECMO的先决条件. 心肌收缩力受多种因素的影响, 包括完好的心肌细胞间和细胞外的结构, 充分的营养和氧供, 适当的植物神经和神经体液调节, 甲状腺激素信号通路, 以及充分的电解质内环境稳定, 包括心肌细胞的钙离子调控. 心脏表现及心肌的完整性也会受到VA-ECMO的不良影响, 这种影响主要也是心脏负荷状况的改变所引起的[29].
改善心肌本身的收缩力的治疗干预在于优化心脏的负荷状况(参见“B: 血压和负荷状况”), 心肌的氧耗及使用特定的治疗. 并没有随机对照研究评估正性肌力药物对VA-ECMO撤机成功率的影响. 而观察性研究发现接受VA-ECMO治疗患者也提示去甲肾上腺素和病死率风险升高相关[30], 使用左西孟旦VA-ECMO撤机成功的几率增加1.6倍[31]. 另外系列病例也提示使用磷酸二酯酶-III-抑制剂(米力农或是依诺昔酮), 联合低剂量的β受体阻滞剂能增加VA-ECMO撤机的成功率[32]. 总之强心扩血管药物可能可以增加脱机的成功率.
另外也应当尽量优化冠状动脉氧含量和心肌氧需求. 对于VA-ECMO撤机失败下合适的输血阈值和血红蛋白目标目前尚不明确.
对于C: 收缩力和冠状动脉的诊断和治疗推荐
- 1、考虑使用扩血管强心治疗和心力衰竭治疗, 同时避免这些药物潜在的不良反应.
- 2、对于撤机失败的病例予以优化动脉血氧含量. 注意在右上肢测定动脉血氧饱和度因其最能一致的反应冠状动脉血氧合水平.
- 3、降低心肌的氧需求, 控制发热, 呼吸功和寒战, 尽量降低全身氧摄取.
- 4、当出现心肌缺血及/后冠状动脉状况不明时, 需要考虑施行(重复)冠状动脉造影术. 当发现严重的冠状动脉狭窄时需要行血管再通治疗.
D: 机械性功能障碍
一些机械性的问题也会引起心功能障碍. 其中包括心包填塞, 室间隔破裂(ventricular septal rupture, VSR), 新发的严重二尖瓣返流(心肌梗死后的腱索断裂)以及二尖瓣前叶在收缩时的前向运动(systolic anterior motion, SAM)引起严重的二尖瓣返流和左室流出道梗阻(left ventricular outflow tract obstruction, LVOTO).
行VV和VA-ECMO支持患者中心包填塞发生率约为2%[34]. 心肌梗死或心脏手术, 心肌周围炎[35], 游离壁破裂[36], 置入导管时的心脏穿孔[34]或是心脏手术后心包囊内血栓的累积都会继发反应性心包炎, 引起心包填塞. 在VA-ECMO时识别心包填塞可能被忽略, 因为传统的征象会被VA-ECMO建立的并行的体外循环所缓解. 临床怀疑心包填塞联合心包渗出或是血栓时需要立即引流心包渗出. 引流后患者预后相对较好, 撤机成功率和在院生存率分别为82%和73%[34].
室间隔破裂引起VA-ECMO时持续的休克在临床上和心肌梗死引起左右心室衰竭很难区分. 当心梗不久后出现新的右心室扩张或是衰竭, 新的响亮的心脏杂音, 或是肺动脉导管提示显著的血氧饱和度和/或心输出量增加但持续性终末脏器低灌注时则需要怀疑. VA-ECMO支持治疗患者出现VSR的30天病死率从43%到57%不等[37].
严重的左心衰竭常规可观察到临床显著的二尖瓣返流并会对VA-ECMO的撤机产生不良影响. 同时也可能联用Impella以利于VA-ECMO的撤离, 设备相关二尖瓣返流也可能为其并发症[38]. 在一项ELSO注册研究中也发现42名乳头肌断裂继发的严重二尖瓣返流的患者接受VA-ECMO的支持[37]. 在院生存率接近43%[37], 治疗方式包括瓣膜修复或替换[39]及经皮修复[40].
VA-ECMO能有效救治肥厚性心肌病[41]和应激相关心肌病[42]引起的左心室流出道梗阻(LVOTO)导致的心源性休克. 由于LVOTO会引起左心室前负荷和后负荷的增加, 而VA-ECMO会缓解其严重程度[27]. 同样LVOTO对VA-ECMO撤机失败造成的影响可能会被低估, 在高VA-ECMO血流时甚至被忽视. 因此在撤机试验时存在该情况或是在撤机后立即出现心源性休克时需要特别注意. 当VA-ECMO的撤离取决于LVOTO并且保守手段失败时, 必须考虑经皮腔内室间隔化学消融术, 或是外科心肌切除联合或不联合二尖瓣成型/替换[41].
对于D: 机械性功能障碍的诊断和治疗推荐
– 当VA-ECMO撤离失败时, 积极解决临床程度显著的心包渗出/血栓, VSR, 重度二尖瓣返流和LVOTO.
- 1、注意心包填塞, VSR和LVOTO所引起的功能性后果可能会被VA-ECMO本身的血流动力学效应所掩盖.
- 2、对于引起的血流动力学障碍的心包渗出/血栓, 撤机试验前考虑引流和外科探查.
- 3、对于VSR在初步稳定期后考虑外科修复或是经皮闭合术.
- 4、对于新发的重度二尖瓣返流, 考虑手术瓣膜修复/替换或是经皮修复.
- 5、对于肥厚性心肌病引起的LVOTO, 考虑室间隔化学消融, 手术心肌切除.
E: 心外因素
心肌功能受大量心外因素的显著影响, 可分为以下几类:
机械通气
大部分接受VA-ECMO治疗的患者需要机械通气, 因为严重的心源性休克通常伴有明显的呼吸功能不全. 虽然VA-ECMO可以提供额外的呼吸支持, 机械通气的优化管理不可或缺, 对气体交换的影响取决于双重循环的程度以及氧合的差异[43-45]. 这包括了重视心肺交互, 以及保证足够的呼吸力学, 以及对抗肺水肿的静水压, 而后者是VA-ECMO常见的严重并发症[46-48].
目前的文献并未提供清晰的证据指导VA-ECMO时日常机械通气实践. 但基于病理生理学的考量有助于设定优化VA-ECMO撤离时需要考虑的临床目标.
呼气末正压通气 寻找最佳的呼气末正压(PEEP)需要权衡对左右心室前后负荷的影响, 同时尽量减轻肺水肿和肺不张. 约10 cmH2O的高-正常PEEP一般是合适的妥协, 同时结合左右心室的大小和功能的心脏超声和血流动力学监测有助于确定个体患者的最佳选择. 而当心脏射向升主动脉和冠状动脉的血流逐渐增加时, 肺本身的气体交换功能则显得尤为重要. 同样在没有水肿和不张的情况下低-正常的PVR有益于右心室功能.
肺保护性通气 VA-ECMO相关肺损伤在临床中十分重要, 由不同的机制和临床问题所介导, 不仅包括静水压升高的肺水肿, 还包括炎症, 肺泡出血, 血栓栓塞以及缺血, 而后者则是体外循环血流速高时经过肺血流降低所引起的并发症[49]. 这都提示在急性呼吸窘迫综合征(ARDS)中广泛接受应用的肺保护性通气应当成为目标, 而气体交换则需要充分保证能弥补VA-ECMO的功能性右向左分流. 随着靠近预定VA-ECMO撤机时间, 患者的气体交换不应当严重依赖于膜氧合器, 而是通过机械通气达到足够的气体交换.
内分泌的效应
甲状腺功能亢进[50]和甲状腺功能减退[51]都会引起心力衰竭需要ECMO支持. 但目前尚不明确何种程度的甲状腺激素改变会导致VA-ECMO撤离失败. 由于在大多数危重患者中可观察到在没有下丘脑-垂体-甲状腺轴疾病(所谓非甲状腺疾病, non-thyroidal illness)的情况下有甲状腺激素水平的改变, 这显得尤为有意义[52]. 没有明确的证据下我们建议对于发生VA-ECMO撤离失败的患者考虑纠正严重改变的甲状腺激素水平.
肾上腺功能不足可加剧心力衰竭[53, 54], 甚至在严重的病例中需要VA-ECMO的支持[51, 55]. 但目前尚不清楚到何种(相对)程度的肾上腺皮质功能不足会对ECMO撤离失败产生影响. 当患者存在无法解释的大量升压药物和典型的肾上腺功能不足时, 有必要进行彻底的内分泌方面的诊断检查. 个别病例中嗜铬细胞瘤通过儿茶酚胺能应激也能解释心源性休克需要ECMO支持治疗[56].
炎症状态
随着ECMO支持时间延长发生感染的几率增加, ECMO支持患者约14%至65%的患者报道会发生感染[58]. 支持超过48小时的部分患者中感染发生率最高的是呼吸机相关肺炎(VAP: 55%), 之后是血流感染(18%), 导管感染(10%)和纵隔感染(11%). 一些研究发现ECMO支持过程中发生感染和撤机失败及在院病死率风险显著升高相关[59].
电解质紊乱
明显的低钙血症有报道会发生一过性的充血性心力衰竭[60, 61]和心源性休克[62]. 同样既往研究也表明在体外循环过程中或者结束后立即予以静脉补钙能改善心输出量和平均动脉压[63, 64]. 血清钙浓度和补钙对ECMO支持时心肌功能的影响尚未进行评估. 严重的低钾血症和低镁血症会放大心律失常的风险[65]. 另一方面, 高钾血症可能会引起严重的传导组织和严重的心率过缓.
对于E: 心外因素的诊断和治疗推荐
- 1、呼吸机设定的目的为优化心脏负荷状态, 同时也改善右-左心室的交互作用.
- 2、对于有活动性感染, 考虑在彻底控制感染源和抗生素治疗后再次行撤机试验. 如果无法延迟撤机, 尽量控制发热和寒战.
- 3、对于明显的甲状腺功能减退, 补充甲状腺激素.
- 4、怀疑肾上腺功能不足时进行彻底的内分泌诊断检查, 并相应补充盐皮质激素及糖皮质激素.
- 5、对于心室收缩功能不全, 考虑优化血钙水平(> 1.0 mmol/L)
- 6、维持血钾(> 4.0 mmol/L)和血镁(> 1 mmol/L)正常高水平.
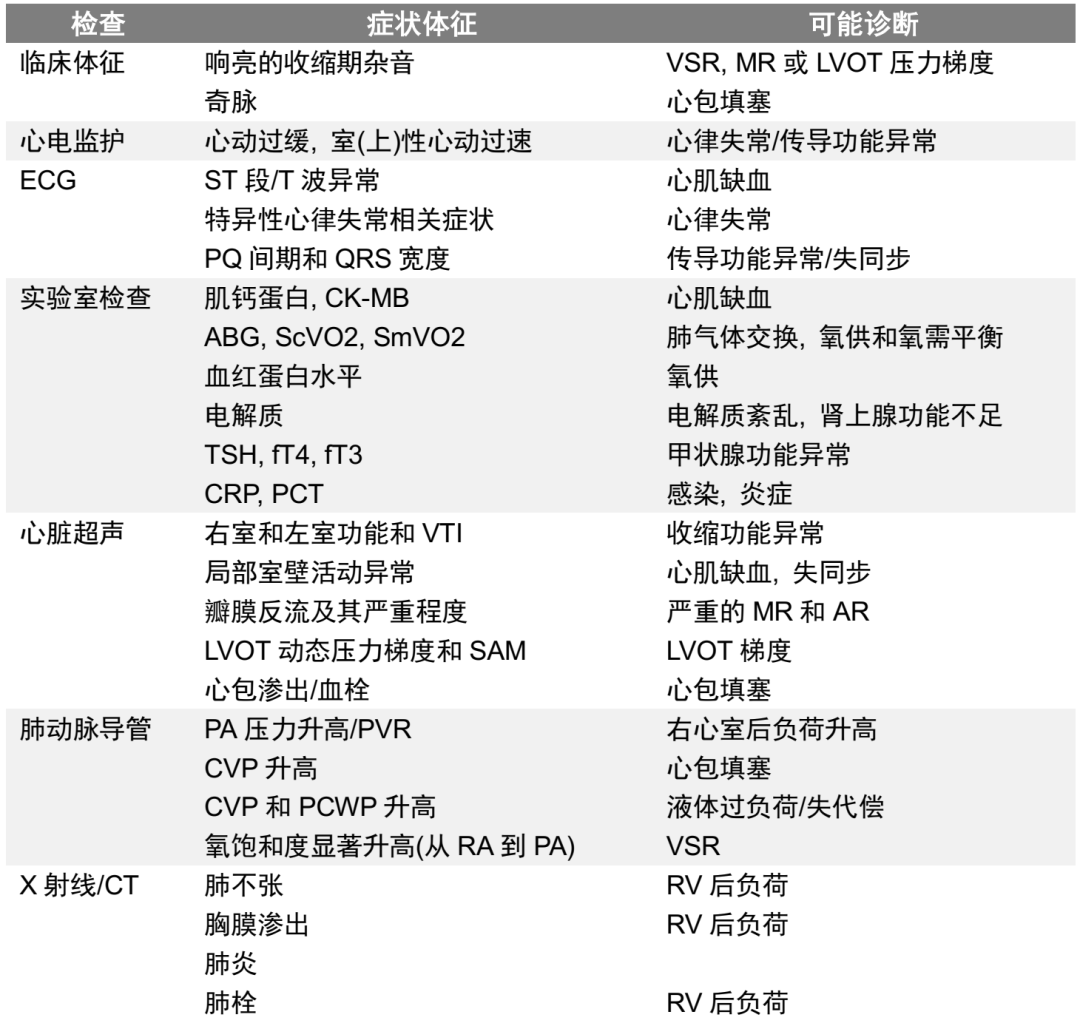
在讨论完以上各种因素后我们列出了检查清单(表1), 能够用于VA-ECMO支持撤离困难的患者. 对于特定的患者, 这些不同检查的顺序的意义可能有所不同.
未来的方向
目前VA-ECMO撤离成功率低强调了将努力方向集中在可能改善未来患者预后的因素的必要性, 这包括:
- 1、需要讨论统一的VA-ECMO撤离失败的定义, 以便最大程度提高相关研究的效率和可比性.
- 2、需要大规模的观察性研究, 包括高质量的详细数据结合每位患者的反复测量, 因为(1)改善患者的选择, (2)明确撤机失败和LVAD成功植入的预测因素, 以及(3)评估撤机失败的高危因素及其影响.
- 3、最后, 很明显目前对于研究不同的治疗干预手段对于提高撤机成功率的随机对照研究数据缺乏. 这包括(1)VA-ECMO撤离的最佳时机, (2)左室去负荷设备的影响, 以及(3)使用强心扩血管药物促进VA-ECMO撤离的类型和剂量.
结论
虽然近年来VA-ECMO的应用大幅增长, 但很多患者仍无法撤离VA-ECMO且1年的病死率约为50%. 本文阐述了阻碍VA-ECMO成功撤离的重要潜在因素. 对于特定患者的结构化方法(ABCDE)和评估有助于明确高危因素. 将来的工作需要将当前对VA-ECMO撤离失败的理解进一步扩展, 并明确治疗干预手段以优化这些因素, 改善撤机成功率.
特别申明:本文为转载文章,转载自重症文献翻译转运站 ,作者转运站小蜜蜂,不代表贪吃的夜猫子立场,如若转载,请注明出处:https://mp.weixin.qq.com/s/k8aSAIrY5z2Ka2UdItZnvw

 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫