20世纪初,腰椎穿刺术问世不久,德国神经科医师Max Nonne描述了一种见于脑脊液(CSF)压力升高患者,伴有视盘水肿的头痛综合征。他将该疾病命名为“假性脑瘤”,因为所有患者均未发现脑肿瘤。该名称沿用至今,但基本上已经被“特发性颅内高压”取代。本文综述了当前对该疾病的认识,重点探讨硬脑膜静脉窦狭窄的重要性及新型治疗方案。

临床诊断
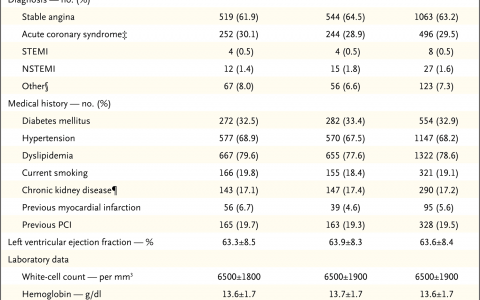
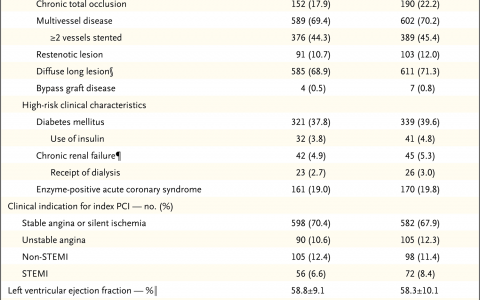
特发性颅内高压患者有95%以上为肥胖的育龄女性。男性罕见发病,原因不明。即使在肥胖女性群体中该病亦属罕见,在体质指数(体重[千克]除以身高[米]的评分)超过30的女性中患病率只有约1/500。随着肥胖率激增,该病患病率呈上升趋势。发病前常有近期体重增加情况。特发性颅内高压可发生于儿童,但青春期前与肥胖和女性之间的关联性比较不明显。
确诊前需排除其他导致颅内压(ICP)升高的潜在病因。尤其对于不符合典型临床特征的患者,应寻找其他病因。四环素类抗生素和维甲酸类药物(维生素A及相关化合物)可诱发罕见的继发性颅内高压。脑静脉窦血栓形成、硬脑膜动静脉瘘等血管疾病可能出现与特发性颅内高压相似的表现。
头痛是最常见的首发症状,84%患者报告此症状。约半数患者描述头痛呈持续性或每日发作。偏头痛病史常见。其他突出症状包括短暂性视力模糊(68%患者)、颈背部疼痛(53%)、搏动性耳鸣(52%)、视力减退(32%)及复视(18%)。特发性颅内高压偶尔会导致颅底CSF漏,进而引发鼻漏或浆液性中耳炎。
视盘水肿是最突出体征,通常也是唯一体征。除偶见第六对颅神经麻痹外,神经系统检查结果通常正常,但也有报道出现非典型表现,包括其他颅神经病变。由于特发性颅内高压患者的症状易与常见疾病混淆,且当ICP仅轻度升高时临床表现不典型,或未进行眼底检查,因此该疾病有时会被漏诊。
眼部表现
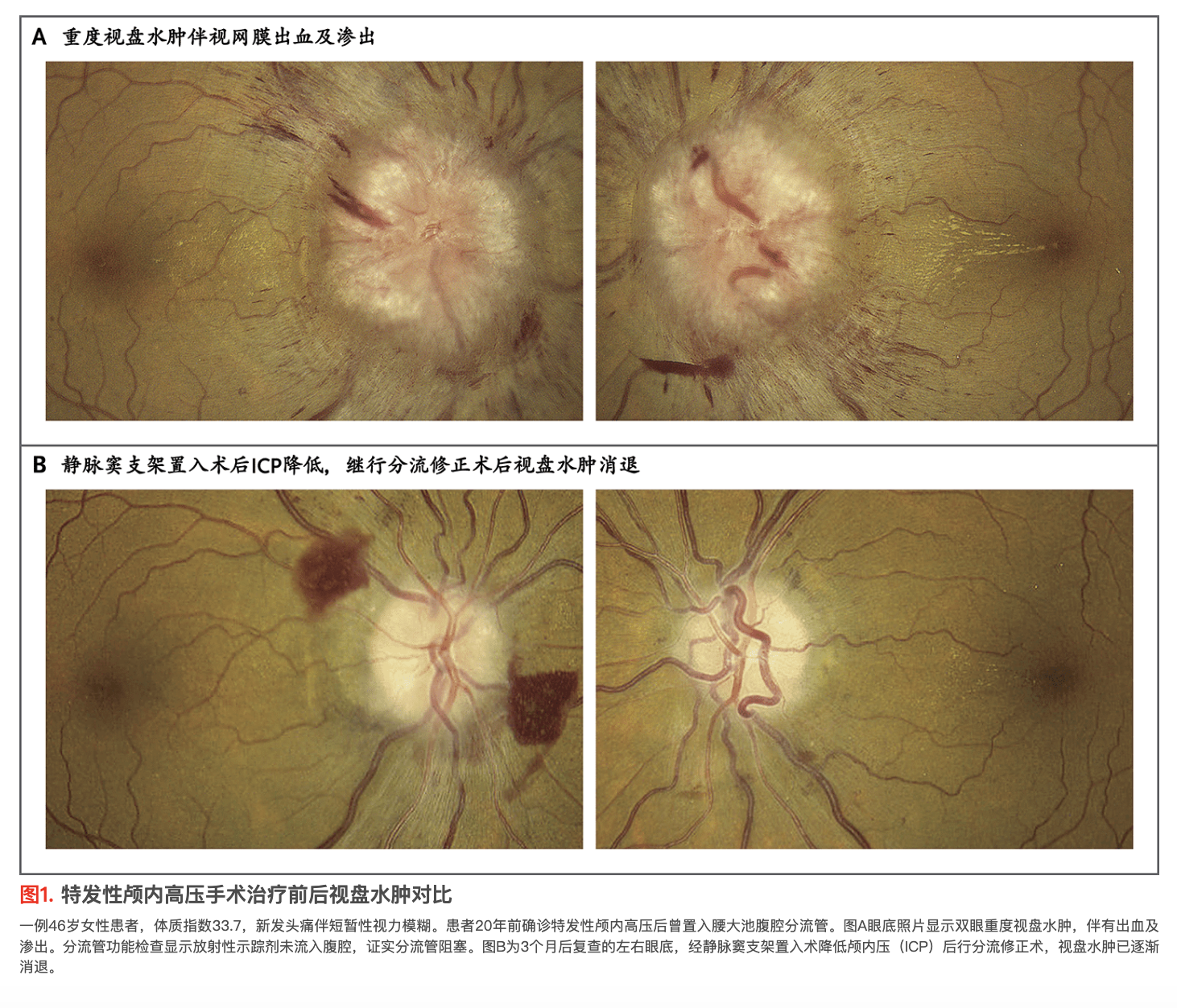
视盘水肿是由ICP升高导致(图1)。许多医师发现用检眼镜观察视盘困难,尤其在未药物散瞳时。自动对焦眼底相机无需散瞳即可成像,为急诊科筛查视盘水肿提供了可行方案。疑似视盘水肿患者应尽快转诊至验光师或眼科医师处,以确认该表现并排除其他视盘水肿病因,例如由视盘玻璃膜疣引发的假性视盘水肿。
视盘水肿导致的视力减退常从视野周边逐渐蔓延,初期可能不易察觉。除非视盘渗出的液体蔓延至黄斑区,否则中心视力通常最后受累。任何程度视力下降都提示视神经已遭受严重损伤。由于特发性颅内高压最严重的威胁是不可逆性失明,因此及时干预至关重要。计算机视野检查较对比视野检查更灵敏且结果更具可重复性,对评估视神经功能及指导治疗具有重要价值(图2)。
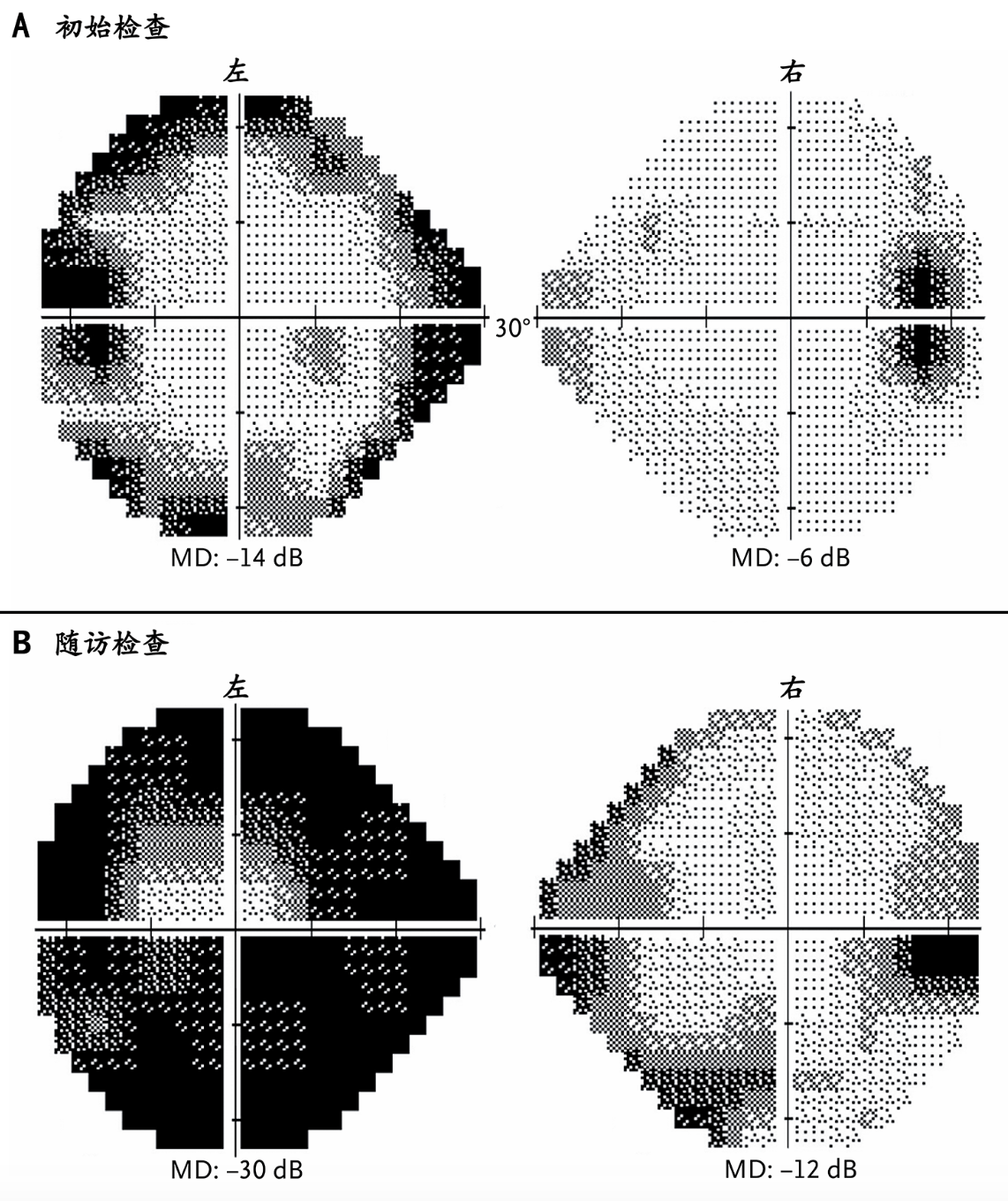
A显示图1患者在眼底成像当天进行的初始Humphrey视野检查,可见双侧盲点扩大及左眼视野周边缩窄。双眼视力均为20/20。图B显示3个月后的随访视野检查,可见左眼视野重度缩窄,右眼视野中度缩窄。右眼视力维持20/20,左眼视力在支架置入术后逐渐下降至20/800,经分流修正术后恢复至20/60。图中标注了每只眼睛视网膜敏感度相对于正常视野的平均偏差(MD,单位为分贝[dB])。-30dB表示视网膜平均敏感度降低3个对数单位。
未见视盘水肿提示ICP正常,但不能排除特发性颅内高压。至少5%的患者(尤其是ICP仅轻度升高者)仅有轻微视盘水肿或无视盘水肿21。眼底检查有时难以得出定论,因为生理性视盘边缘模糊(无视盘水肿)的健康人群与早期或轻微视盘水肿患者常难以区分22。光学相干断层成像可评估视盘周围视网膜神经纤维层厚度,但该测量值仍无法完全消除视盘水肿诊断的不确定性。值得庆幸的是,视盘可以耐受轻度视盘水肿,对视力造成的风险较小。对于多数新确诊的特发性颅内高压患者,主要挑战是如何控制头痛。
视盘水肿严重程度需结合视神经萎缩程度综合判断。如果ICP持续失控,肿胀视盘最终会消退并演变为萎缩性平坦视盘。少数患者因长期未得到诊断的特发性颅内高压导致视神经损伤,就诊时已出现晚期视力减退,视盘颜色变淡且肿胀不明显。
神经影像学检查及其对病理生理学的启示
“假性肿瘤”这一名称恰如其分,因为要诊断特发性颅内高压,必须排除颅内肿块。虽然计算机断层扫描(CT)可能足以达到这一目的,但在评估疑似特发性颅内高压导致视盘水肿的患者时,磁共振成像(MRI)优于CT。在注射钆造影剂前后获取序列图像,并实施磁共振静脉造影。ICP升高导致的影像学表现包括视盘向玻璃体腔突出、眼球后部变平、CSF引起视神经鞘扩张、小脑扁桃体向下移位以及部分空蝶鞍。最值得注意的发现是横窦狭窄(图3),因为其对特发性颅内高压病理生理学具有重要意义,在一个病例系列中94%的患者存在该表现25。横窦狭窄通常发生于双侧,或发生于单侧且另一侧横窦发育不全。尽管横窦狭窄并非特异性指标,但在无特发性颅内高压的人群中,该表现发生率低于5%。
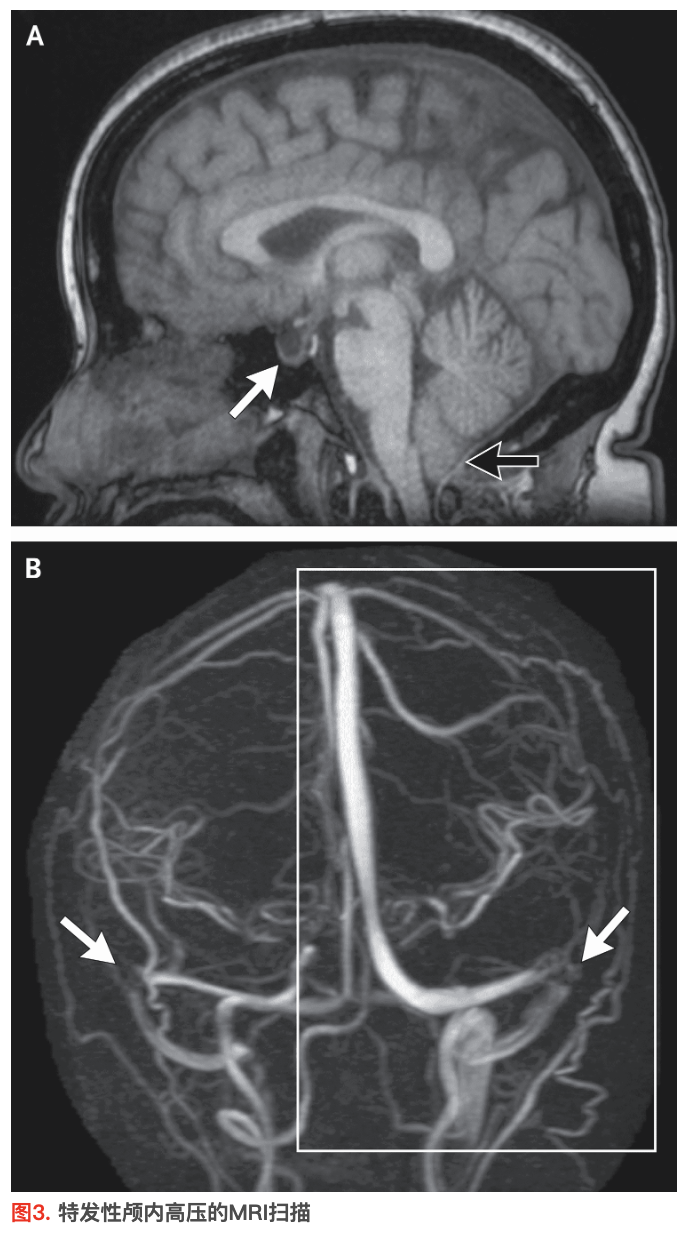
图A为图1患者的MRI(非造影矢状位T1加权图像),可见特发性颅内高压典型表现:部分空蝶鞍(白色箭形)和小脑扁桃体向下移位6 mm至枕骨大孔下方(黑色箭形),部分原因可能是腰大池腹腔分流引发的压力梯度。图B为非造影三维相位对比磁共振静脉造影图像,可见双侧远端横窦狭窄(箭形)。矩形框内区域为图5所示静脉系统部分。
在特发性颅内高压患者中观察到的硬脑膜静脉窦狭窄现象催生了一种理论:该疾病是由正反馈循环驱动,进而产生临床表现(图4)。该过程始于躯干肥胖导致的颈静脉压升高。上述静脉压升高传递至颅内硬脑膜静脉窦,减小了硬脑膜静脉窦正常吸收CSF的压力梯度。为维持CSF清除速率,ICP随之升高。ICP升高压迫硬脑膜静脉窦,尤其在横窦与乙状窦交界处形成功能性狭窄。该部位的局灶性狭窄加剧脑静脉高压,进而推高ICP。该机制的直接佐证来自静脉测压观察:特发性颅内高压患者在狭窄远端横窦处呈现压力梯度,而通过腰椎穿刺快速清除大量CSF可缓解此现象。此外,对视盘水肿实施成功药物治疗可逆转横窦狭窄。
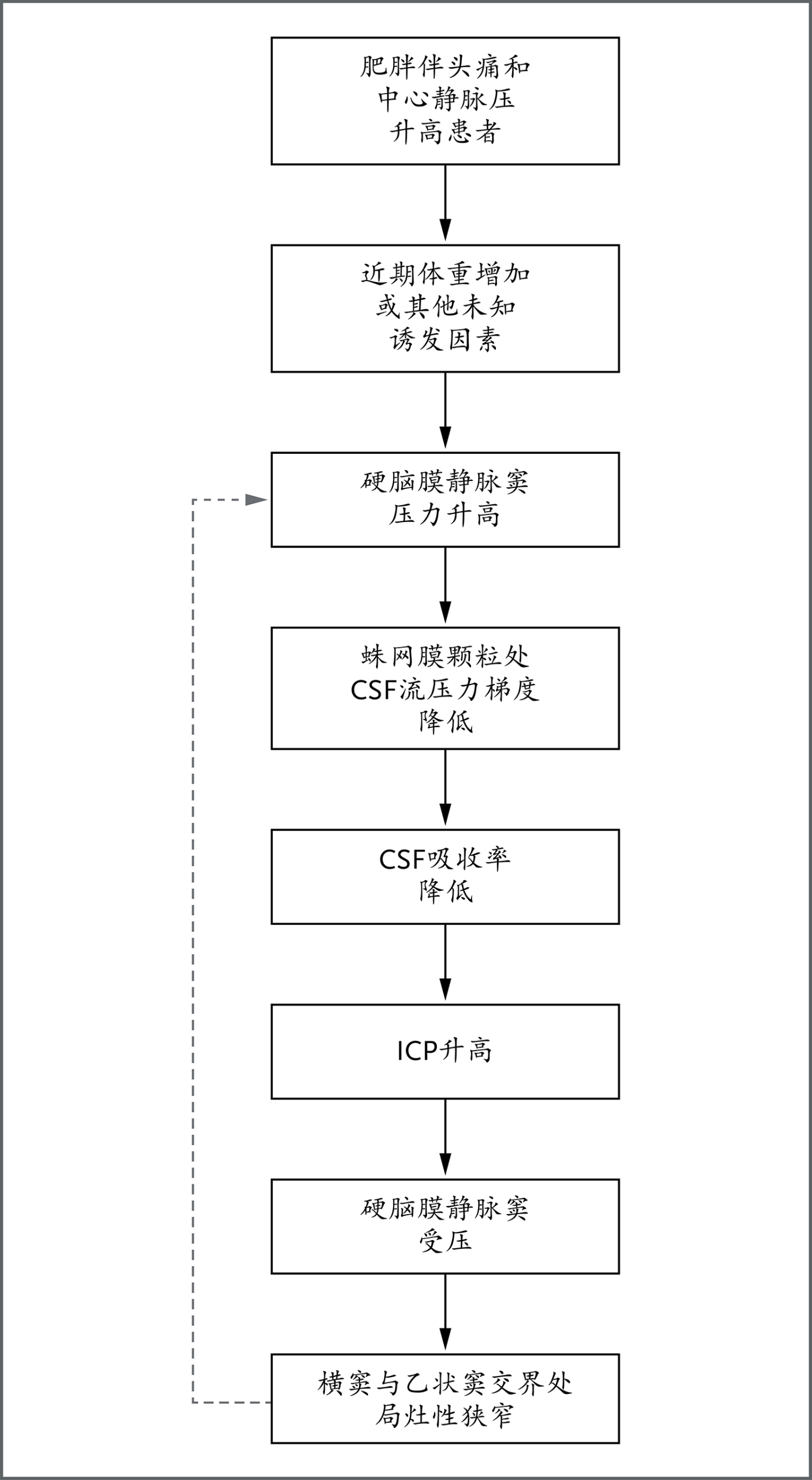
体重增加导致中心静脉压升高,进而升高硬脑膜静脉窦压力和ICP。升高的ICP压迫硬脑膜静脉窦,加剧静脉高压。横窦与乙状窦交界处出现局灶性狭窄的原因尚不明确。减重和乙酰唑胺可缓解病情,推测是通过逆转驱动颅内高压的正反馈循环实现。CSF表示脑脊液。
该理论暗示,即使并非大多数,也有许多特发性颅内高压患者存在亚临床病变,表现为ICP在正常与升高阈值间波动时引发的间歇性头痛及其他压力相关症状。肥胖人群的中位ICP较非肥胖人群高出10%~15%,这一观察结果支持此观点。在庞大的高危人群中,少数患者从代偿状态转为显性特发性颅内高压的诱发机制仍不明确。部分病例可能是由近期体重增加导致。
如前文所述,在被转诊接受神经影像学检查的患者中偶尔可见提示ICP升高的MRI表现,有时临床医师并未怀疑特发性颅内高压。因此,神经放射科医师已成为将患者转诊至眼科和神经科医师处,以排除视盘水肿的重要渠道。如果眼底检查正常,且患者符合临床特征,同时神经影像学证据有力支持ICP升高的表现,则必须考虑不伴有视盘水肿的特发性颅内高压诊断。
CSF压力测量的诊断与治疗意义
如果神经影像学已排除肿块或静脉血栓,则通常会进行腰椎穿刺,以测量腰椎蛛网膜下腔初压并采集CSF样本。如果患者取侧卧位时压力计读数高于25厘米水柱(18.4 mm Hg),且CSF成分正常,临床特征符合,则可诊断为特发性颅内高压。存在不确定性的原因包括: 偶见特发性颅内高压患者初压低于25厘米水柱,且部分病例系列显示2.5%健康人的初压高于该数值。
腰椎穿刺仅能获取单次压力读数,而ICP如同血压般会随活动与体位变化大幅波动。由于肥胖问题,对特发性颅内高压患者进行腰椎穿刺可能很困难,不当体位、腹压、用力过度及针头位置不当均可能导致读数不准。此类患者常被转诊至放射科医师处,后者通常采用俯卧位实施腰椎穿刺。采用俯卧位进行腰椎穿刺时,需将针头长度(9 cm)加至压力计液柱高度。如果未执行此步骤,报告的ICP值可能不准。
尽管腰椎穿刺被视为诊断特发性颅内高压的必要手段,但对特定患者群体可合理省略该操作。当只有轻度视盘水肿或无视盘水肿时,腰椎穿刺初压多在20~30厘米水柱范围内。该数值区间的诊断意义有限,因为其与健康人群压力值存在重叠。有观点认为,如果患者临床表现典型,则可省略腰椎穿刺直接启动治疗;如果MRI显示横窦狭窄、部分空蝶鞍且无脑膜增强,并且无提示其他诊断的警示征象,则可直接启动治疗41,42。一项回顾性病例系列研究表明,因未进行CSF分析而漏诊无菌性脑膜炎(其表现与特发性颅内高压相似)的风险低于1%。
当视盘水肿达到中度至重度时,腰椎穿刺具有诊断意义,因为此时脑脊液压力读数往往明显升高。通常需抽取比较大量CSF(如30~40 mL),以快速降低ICP,保护视盘免受损伤43。通常无需测量终压。穿刺硬膜形成的孔洞常会持续引流脑脊液长达一周。当ICP升高时,上述引流具有治疗作用,因此除非出现顽固性体位性头痛且明确由ICP降低引起,否则应避免使用血补片。需检测CSF的葡萄糖、蛋白水平及细胞计数。如果分析结果正常,则无需进一步检测CSF。
除重度视力减退时的临时措施外,反复腰椎穿刺并非管理ICP升高的可行策略。一旦腰椎穿刺确诊特发性颅内高压,重复测量的意义有限。例外情况是视神经萎缩患者无法配合视野检查时。这种情况下,眼底检查可能显示仅有轻微视盘水肿或无视盘水肿,但隐匿性视力减退仍可能持续进展。确认ICP得到充分控制的唯一途径可能是通过腰椎穿刺测量,有时需反复操作。极少数情况下需进行持续性侵入性颅内监测,以明确诊断。
治疗
多数疑似特发性颅内高压患者可在门诊治疗,前提是评估需及时进行。如果出现视力减退,则应转诊至急诊科。该病患者常因保险覆盖范围有限而前往急诊科就诊, 其中黑种人或西班牙语裔患者比例较高,多属低收入群体,且常有抑郁、焦虑病史或与肥胖相关的自尊心受损。对此类患者采取尊重的态度至关重要,尤其在涉及体重管理、头痛药物滥用等敏感议题时,这样有助于建立良好医患关系。
治疗启动后,需定期评估视力、视野及眼底状况,以监测视神经功能。检查可由验光师执行并向医师反馈结果, 检查频率应根据患者病情严重程度调整。
药物治疗
减重联合口服乙酰唑胺是特发性颅内高压的主要治疗手段。乙酰唑胺通过抑制介导CSF分泌的碳酸酐酶发挥作用。常规剂量为每日2~4次,每次500 mg缓释胶囊。在数天内逐渐增加剂量可减轻恶心和手足感觉异常等副作用。该药物妊娠期使用安全。对于无其他健康问题的患者,我通常不进行电解质水平监测。另一种碳酸酐酶阻滞剂托吡酯在小型非随机试验中可有效降低ICP,其机制可能涉及抑制碳酸酐酶和减轻体重56。糖皮质激素无效,即使面临灾难性视力减退时亦然。特发性颅内高压患者无需停用口服避孕药。
减重可改善特发性颅内高压患者的病情,但仅靠饮食和运动难以实现并维持减重效果57。一项随机试验表明,减重手术优于减重项目,接受手术患者在12个月内平均减重21.4 kg,ICP平均降低7.2厘米水柱58。胃旁路手术较袖状胃切除术或胃束带术更有效,胃旁路手术使患者平均减重36.0 kg,ICP平均降低15.5厘米水柱59。
胰高血糖素样肽-1(GLP-1)激动剂及抑胃多肽激动剂是减重手术的替代方案。除减轻体重外,GLP-1药物在动物模型中似乎还可通过抑制CSF分泌的方式降低ICP60。目前前瞻性随机试验数据有限,尚未证实GLP-1激动剂对特发性颅内高压的疗效61。然而,减重手术的疗效强烈提示这些药物可能从根本上改变特发性颅内高压的疾病管理模式。我们采用口服司美格鲁肽治疗患者时,观察到患者体重在约4个月内下降10%~15%,同时视盘水肿症状消退。所有肥胖合并特发性颅内高压患者在确诊时均应获得GLP-1激动剂及抑胃多肽激动剂治疗机会。每次门诊称重有助于监测体质指数下降趋势。未来随着肠降血糖素受体激动剂通过减重实现特发性颅内高压缓解,治疗该疾病所需的手术干预(详见下文)可能会减少。
手术治疗
少数患者在症状出现仅数日或数周后出现剧烈视力减退、暴发性视盘水肿及ICP升高。此类病例支持以下理论:特发性颅内高压可能长期潜伏未被察觉,直至硬脑膜静脉窦狭窄导致ICP骤升时才发病(图4)。如果无法在数小时内实施手术,可通过置入临时腰椎引流管争取时间。如果患者已出现视力下降且视力减退速度过快,没有时间等到通过减重和乙酰唑胺逐步减轻视盘水肿,则必须进行手术干预。过度延迟手术将导致永久性视力减退。手术方案有三种:视神经鞘开窗术、硬脑膜静脉窦支架置入术及CSF分流术。手术的唯一目的是防止视力减退。不建议为治疗头痛或搏动性耳鸣而手术,因为根据共识指南,这些症状可通过药物治疗和减重缓解63。
旨在确定特发性颅内高压患者最佳手术方案的随机临床试验因患者招募困难而进展受阻。每种手术方案各有优势,且伴随不同的并发症风险。目前尚未就最佳手术方案达成共识,因此应与患者全面讨论三种选择。
视神经鞘开窗术
在视神经鞘开窗术中,眼科医师于眼球后方视神经鞘处开窗,使CSF流入眼眶,从而缓解视盘水肿。有时对侧眼视盘水肿亦可改善,但通常需行双侧手术。一项研究显示,当该手术用于治疗其他疾病(如前部缺血性视神经病变)时,存在2%的视神经损伤致视力减退风险65。开窗通常在数月内闭合,但神经鞘切口边缘与软蛛网膜间会形成黏连,通过隔离视盘与眼球后蛛网膜下腔的方式,使视盘免受高压影响66。
该手术的主要缺陷在于:除存在术后视神经损伤致盲风险外,无法有效降低ICP67。因此头痛、复视及耳鸣症状常持续存在。如果术后瘢痕未能完全封闭视神经周围蛛网膜下腔,则视力减退可能持续进展。在一项病例系列研究中,35例接受视神经鞘开窗术的患者中,有17例最终需行CSF分流术或静脉窦支架置入术,以保护视力68。
硬脑膜静脉窦支架置入术
实施硬脑膜静脉窦支架置入术时,患者需接受全身麻醉,介入放射科医师首先确认该区域存在明显静脉压梯度,随后将支架穿过影响优势横窦的狭窄部位28,69。该手术的优势在于可纠正解剖学阻塞,而这种阻塞被认为是导致ICP自我强化性升高的核心因素(图4)。在对19个已报道病例系列的汇总分析中,硬膜下血肿或脑内血肿风险较低(0.49%),但有两例死亡报告。该综述同时指出,CSF压力平均下降13.3厘米水柱70。患者术后需服用阿司匹林和氯吡格雷长达6个月,以预防支架内血栓形成。
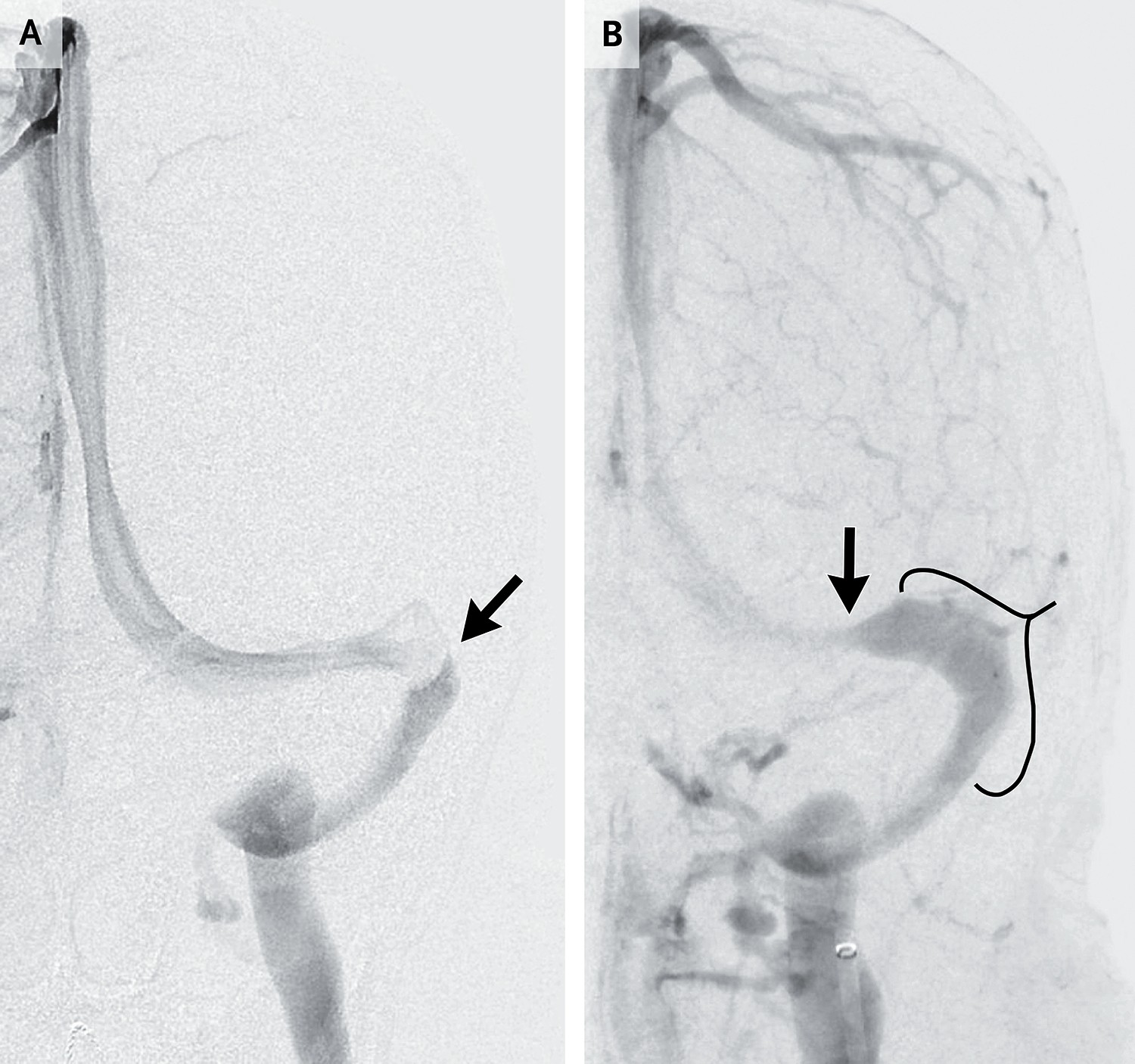
静脉窦支架置入术最严重的局限性是部分患者虽然ICP降低,但未能恢复至正常范围。如果ICP仍然偏高,视觉功能可能继续恶化。由于接受双联抗血小板治疗的患者禁忌腰椎穿刺,因此支架置入术后无法立即检测初压。由于担忧支架疗效不完全,因此许多患者仍需持续服用乙酰唑胺。多项病例系列研究显示,15%的患者出现支架邻近区域新发狭窄(图5)。复发性狭窄表明ICP仍偏高,恰在需要缓解视盘水肿的时刻持续损害视盘。通常可通过二次支架置入术进一步降低ICP,但有时需行CSF分流术才能阻止视力减退。
CSF分流术
尽管静脉窦支架置入术日益普及,但CSF分流术仍是药物难治性特发性颅内高压的标准治疗方案。分流术可立即将ICP降至正常范围,保护视盘,并且可以停用乙酰唑胺治疗。CSF引流由外部可编程分流阀调节,而置入静脉窦支架的话,医师无法直接控制ICP。腰大池腹腔分流与脑室腹腔分流两种系统具有相似的失败率和并发症73。腰大池腹腔分流避免了导管穿过脑组织带来的微小风险,也无需在颅骨置入连接器械。多数神经外科医师对脑室腹腔分流术的操作经验更丰富,而术中导航成像技术的应用,使导管近端置入特发性颅内高压患者通常较小的脑室变得更为简便。
CSF分流术的主要缺陷是高失败率,通常源于导管阻塞。不同研究因方法和随访时间不同而存在结果差异,但通常有20%~40%的病例需行修正术。分流管失功往往是在置入后短期内发生,且易反复失功75,76。分流管失功(实际发生或有潜在风险)是导致急诊就诊的主要原因。急性分流管阻塞发生后,视盘水肿至少需一周才显现,如果视盘已萎缩则可能永不出现,因此眼底检查可能无异常表现。
病情评估需结合神经影像学检查、分流管功能检测,有时还需腰椎穿刺。基于经验丰富的治疗中心的病例系列,有观点认为,由擅长治疗特发性颅内高压的神经外科医师实施手术,并采用腹腔镜置入腹膜导管,可提高分流术成功率75。当CSF分流管运行正常且无故障时,可以最可靠地阻止特发性颅内高压导致的视力减退。然而,鉴于CSF分流管易发生功能障碍,部分神经外科医师转而采用静脉窦支架置入术也就不足为奇了。
结论与未来方向
肥胖患病率的上升增加了特发性颅内高压的高危人群。当只有轻微视盘水肿或无视盘水肿,且ICP仅略高于正常范围时,诊断难度较大。如果能开发出准确测量ICP的无创技术,将有助于评估疑似特发性颅内高压引起的头痛患者。神经影像学揭示了该病机制的关键线索:远端横窦的局灶性狭窄会激活正反馈循环,进而推高ICP。通过GLP-1激动剂或抑胃多肽激动剂减轻体重,配合乙酰唑胺减少CSF生成,可打破该循环。当视盘水肿严重到可能导致不可逆视力减退时,需紧急实施手术以防止失明。目前亟需开展随机对照试验,确定两种最常见手术方式(CSF分流术与静脉窦支架置入术)的优劣。重度特发性颅内高压患者的最佳治疗方案较为复杂,即使接受规范治疗仍可能出现永久性视力受损。
特别申明:本文为转载文章,转载自NEJM医学前沿,不代表贪吃的夜猫子立场,如若转载,请注明出处:https://www.nejmqianyan.cn/article-info?permalinks=YXQYra2404929

 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫