凝血功能异常在重症监护室(ICU)中十分常见,且始终与不良预后相关。这类异常包括脓毒症诱导的凝血病(SIC)、弥散性血管内凝血(DIC)、创伤诱导的凝血病、肝脏相关的止血功能异常以及抗凝治疗相关的凝血异常,所有这些异常都可能引发出血、血栓形成、器官功能障碍甚至死亡。
这篇简短的综述为解读ICU 常见临床场景下的异常标准凝血功能检测结果提供了实用方法(表 1)。先进的止血功能检测方法不在本综述的讨论范围内。
床旁解读的核心原则
在缺乏活动性出血、血栓形成等临床相关表现的情况下,不应纠正异常的凝血功能检测结果。孤立性的检测异常,如凝血时间延长或D – 二聚体升高,在危重症患者中十分常见,仅凭这些指标本身,不足以作为采取纠正性干预措施的依据。这一原则应指导所有ICU 临床场景下的检测结果解读。
标准凝血功能检测的适用与局限
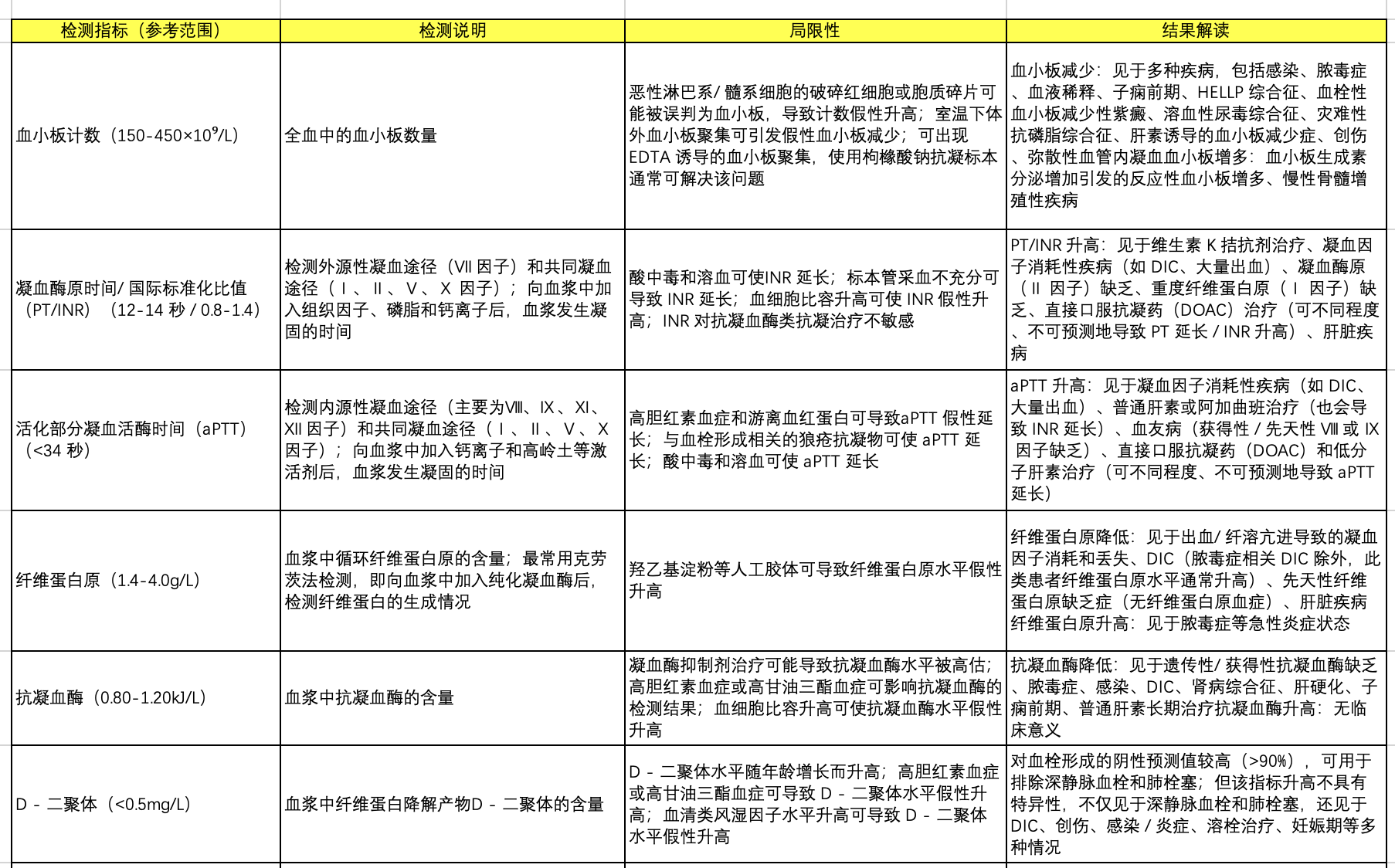
血小板计数、凝血酶原时间(PT /国际标准化比值 INR)、活化部分凝血活酶时间(aPTT)、纤维蛋白原、D – 二聚体等标准凝血功能检测,最初是为检测凝血因子缺乏而研发的,并非为反映危重症患者的整体止血平衡状态设计,因此其在ICU 中的解读存在重要局限性。
例如,aPTT延长在血栓前状态下,可能反映的是狼疮抗凝物的存在,而非出血风险;而炎症反应可能通过使Ⅷ 因子升高,导致 aPTT 缩短。PT/INR 延长可能反映肝脏合成功能下降、血液稀释或凝血因子消耗,而非患者使用了维生素 K 拮抗剂。反之,PT/aPTT 结果正常并不能排除存在具有临床意义的出血或血栓形成风险。
纤维蛋白原是一种急性时相反应蛋白,即便存在凝血因子消耗,其水平也常处于正常或升高状态。危重症患者的D – 二聚体水平几乎均会升高,因此应动态解读该指标。
主要ICU 临床场景下的检测结果解读
脓毒症诱导的凝血病(SIC)与弥散性血管内凝血(DIC)
SIC的诊断标准为血小板计数异常、PT/INR 异常并合并器官功能衰竭 [1],约45% 的脓毒症患者会发生SIC,且该病症与死亡率升高相关 [2]。当病情进展为显性DIC时,患者死亡率会进一步上升(与未发生DIC 的患者相比,死亡率约升高 3 倍)[3]。
标准凝血功能检测结果反映了炎症反应、内皮细胞活化与凝血功能之间的复杂相互作用。血小板减少和PT 延长在该类患者中较为常见,但不具有特异性;而脓毒症状态下,受急性时相反应的影响,纤维蛋白原水平通常会升高[4]。DIC 的诊断可借助相关评分系统(如国际血栓与止血学会 ISTH 评分系统)[5],但这些评分系统也存在局限性,因为血小板计数、PT、纤维蛋白原和 D – 二聚体水平会受肝功能障碍、炎症反应、血液稀释和药物的影响。
DIC的治疗以支持治疗和对症治疗为主;在脓毒症相关DIC 中,治疗重点主要针对血栓前表型,这类患者通常无明显的显性出血表现 [6-8]。因此,在患者无出血表现时,不建议常规纠正凝血功能异常,且应维持标准的血栓预防措施[9]。
血栓性微血管病(TMA)与 DIC 的鉴别
血小板减少是ICU 中最常见的凝血功能异常,约半数ICU 患者会出现该症状,其最常见的诱因包括脓毒症、肝功能障碍、药物作用和骨髓抑制 [10]。血小板减少是危重症严重程度的重要标志物,且始终与不良预后相关,在感染性休克患者中尤为明显 [11]。血小板减少虽常与出血相关,但也可能提示存在需要紧急治疗的血栓前状态。
血栓性微血管病(TMA)与DIC 在临床表现上存在重叠,但发病机制不同:TMA 会引发伴有裂体细胞的微血管病性溶血性贫血、重度血小板减少,以及肾 / 神经系统损伤,而患者的凝血功能检测结果往往正常。反之,DIC 的核心是凝血因子消耗,表现为 PT 延长,脓毒症相关 DIC 患者的纤维蛋白原水平会升高,且 D – 二聚体水平显著升高。血栓性血小板减少性紫癜(TTP)由 ADAMTS13 重度缺乏引起,而溶血性尿毒综合征(HUS)则由志贺毒素介导或补体系统驱动 [12]。准确鉴别TMA 与 DIC 至关重要,若鉴别失误,会延误针对病因的特异性治疗,血涂片检查和针对性的实验室检测是鉴别诊断的关键。
创伤诱导的凝血病(TIC)
创伤诱导的凝血病的特点为:疾病初期表现为低凝状态,出血风险升高,后续则转为高凝、血栓前状态。尽管TIC 的经典诊断标准为凝血酶原比值≥1.2,但其伴随一系列复杂的凝血功能改变,包括血小板减少、纤维蛋白原降低和 D – 二聚体升高,这些指标变化反映了凝血因子的消耗和纤溶亢进。液体复苏和血制品输注导致的血液稀释,会进一步引发纤维蛋白原降低和PT/INR 延长,因此在解读创伤患者的凝血功能检测结果时,需考虑这一因素。
肝脏疾病与肝硬化
肝脏疾病患者的凝血功能检测结果常出现异常,原因包括凝血因子和抗凝因子的合成均减少,以及血小板生成素分泌减少、脾脏扣押血小板导致的血小板减少。尽管肝硬化病情稳定的患者会表现为PT或INR 和 aPTT 延长,但其止血系统往往处于新的平衡状态。当患者合并脓毒症、出血或血流动力学不稳定时,这种平衡会被打破,其临床表现可能与DIC 相似 [13]。
体外器官支持治疗
体外器官支持治疗会通过血液- 材料表面相互作用、炎症反应和抗凝药物暴露,显著改变患者的止血功能。血小板减少、D – 二聚体升高和凝血时间延长在这类患者中十分常见,这些指标变化反映的是凝血系统持续激活(以及抗凝治疗的影响),而非单纯的出血风险。对体外膜肺氧合(ECMO)患者的 D – 二聚体水平进行连续监测发现,该指标的动态变化趋势而非绝对值,可能更有助于判断患者是否存在持续的血管损伤、纤维蛋白代谢异常和出血风险[14,15]。
这类患者的抗凝监测具有挑战性,因为高胆红素血症、溶血、高甘油三酯血症、抗凝血酶缺乏、Ⅷ因子升高、血液稀释和检测方法的干扰,均会影响抗 Xa 因子活性和 aPTT 的检测结果。实验室检测结果与临床抗凝效果不一致的情况十分常见,因此需谨慎解读检测结果,并结合临床情况和体外循环相关事件进行综合分析。
床旁实践注意事项
单一的检测指标无法反映危重症患者凝血功能的动态变化特点[16],解读结果时应依据整体的指标变化模式、临床背景和连续的检测结果,而非孤立的数值。将检测指标的变化趋势与患者的病情发展轨迹相结合,有助于区分适应性反应与病理性的凝血功能紊乱。对于原因不明的出血或血小板减少患者,标准凝血功能检测结果应作为进一步开展针对性检查的依据,而非盲目采取纠正性治疗的理由,因为仅通过PT/INR 或 aPTT,无法排除免疫介导的凝血因子缺乏和获得性凝血因子缺乏。
未来发展方向
异常的标准凝血功能检测结果在危重症患者中普遍存在,其背后反映了炎症反应、内皮功能障碍、器官功能衰竭和治疗干预之间的复杂相互作用。明确这些检测的局限性、结合临床背景解读结果,且在无临床相关表现时避免盲目纠正凝血异常,是实现合理床旁决策的关键。基于发病机制、以临床表型为导向的解读和治疗方法,仍是平衡ICU 患者出血与血栓形成风险的核心。
原创文章(本站视频密码:66668888),作者:xujunzju,如若转载,请注明出处:https://zyicu.cn/?p=21943


 微信扫一扫
微信扫一扫  支付宝扫一扫
支付宝扫一扫 




